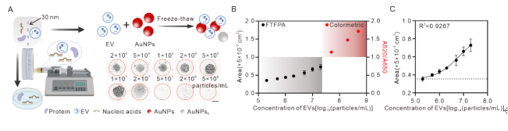
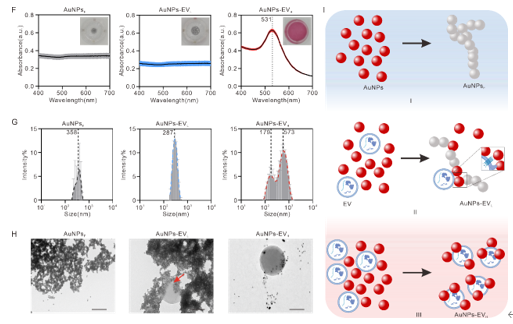
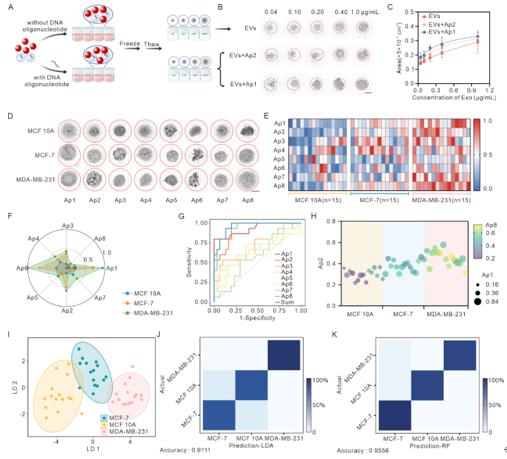
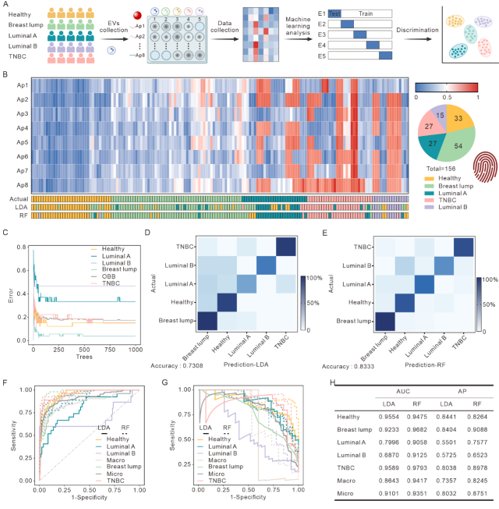
乳腺癌是全球女性最常见的恶性肿瘤之一,早期筛查和及时治疗对提高患者生存率至关重要。然而,现有的诊断方法在精度、速度及成本方面仍存在局限。细胞外囊泡(EVs)因其携带的丰富的信息及非侵入性获取方式,已成为液体活检的重要标志物之一。肿瘤细胞分泌的EVs含有肿瘤特异性蛋白和核酸,它们在乳腺癌不同亚型中呈现独特变化。因此,结合EVs检测与即时诊断(POCT)在癌症诊断和实时监测具有很高的潜力。近日,华中科技大学刘笔锋教授课题组在Small上发表题为“Freeze-Thaw-Induced Patterning of Extracellular Vesicles with Artificial intelligence for Breast Cancers Identifications”的研究论文(2024,Dec 15 :e2408871)。该研究提出了一种基于冻融诱导的金纳米粒子(AuNPs)聚集产生漂浮图案(FTFPA)的检测方法,成功应用于乳腺细胞的EVs分类,并在临床诊断及亚型鉴定中展现了其简便、高效的无创检测优势。华中科技大学生命科学与技术学院谢寒、华中科技大学同济医学院附属湖北妇幼保健院陈冬娟为共同第一作者,华中科技大学生命科学与技术学院刘笔锋教授、陈鹏副教授和李一伟教授为论文通讯作者。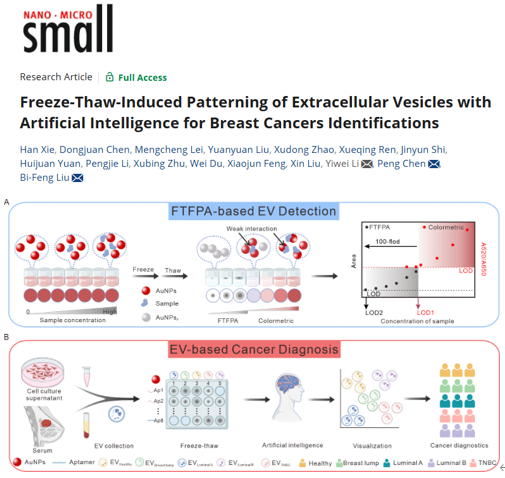
该研究利用AuNPs冻融后形成FTFPA,进行EVs的半定量检测,并利用多种寡核苷酸及人工智能对不同来源的EVs进行分类。首先,研究者探讨了FTFPA用于EVs检测的可行性,结果表明该方法能够有效地半定量分析EVs的浓度。EVs浓度与FTFPA呈非线性正相关,且与传统比色检测方法相比具有更低的检出限,低至1.77×105颗粒/mL。接下来,就冻融诱导的AuNPs形态变化及其与EVs的相互作用机理进行研究。结果表明,没有EVs存在的情况下,冷冻过程中的物理压缩促进颗粒聚集;融化过程的温差引起的对流和增强的表面张力,促进颗粒在溶液表面进行自组装并生成FTFPA。低浓度EVs的磷脂膜与AuNPs结合,导致AuNPs聚集并形成不同的FTFPA,而高浓度EVs则使得AuNPs分布在更多的磷脂膜上,虽然可能发生了部分聚集但保持了更高的稳定性。总之,在目标物浓度较高时,形态看起来相似,而在浓度较低时,由于AuNPs聚集的程度不同而出现差异。随后,通过将不同寡核苷酸的引入进一步提高了FTFPA的分析维度,结合机器学习算法,对不同细胞来源的EVs进行分类诊断,线性判别分析(LDA)和随机森林(RF)模型展示了极高的分类准确性(LDA为0.9111,RF为0.9556)。这些成果表明,FTFPA与机器学习的结合能够显著提高EVs的分类精度,具有早期癌症诊断的潜力。最后,研究者还验证了该方法在临床乳腺癌亚型诊断中的应用。通过对69例乳腺癌患者(包括27例Luminal A型、15例Luminal B型、27例三阴性乳腺癌)、54例乳腺结节和33例健康样本的分析,结合K折交叉验证与机器学习,结果表明RF(分类准确率0.8333)在健康、乳腺结节及乳腺癌亚型分类中表现出优异的诊断性能。华中科技大学刘笔锋课题组近年来在外泌体分离分析及诊疗一体化研究领域取得了一系列进展。之前工作包括:Biosensors and Bioelectronics 227 (2023) 115152;Biomaterials 276 (2021) 121056;Nano Today 37 (2021): 101066.; Advanced Functional Materials 28, no. 18 (2018): 1707360.; ACS applied materials & interfaces 9, no. 33 (2017): 27441-27452.; Nanoscale 9, no. 40 (2017): 15598-15605.; Sensors and Actuators B: Chemical 333 (2021): 129559等。Freeze-Thaw-Induced Patterning of Extracellular Vesicles with Artificial Intelligence for Breast Cancers Identification. Small, 2024,2408871.外泌体资讯网 Small|华中科技大学刘笔锋教授团队:冻融介导细胞外囊泡图案化联合人工智能增强乳腺癌识别