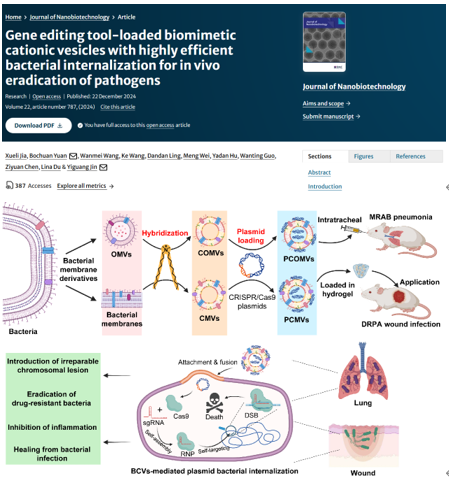
在后新冠肺炎时代,耐药细菌感染发生概率增加,相应的死亡率也有所提升,其中多重耐药鲍曼不动杆菌(MRAB)和耐药铜绿假单胞菌(DRPA)是主要的病原体。尽管抗生素仍是治疗细菌感染的主要手段,但它们的滥用是导细菌耐药性进展的主要原因。抗生素的替代品,如金属离子、抗菌肽、噬菌体等都显示出一定的应用希望;然而它们也存在局限性,如存在毒性、特异性、溶血风险等问题。因此,迫切需要开发新的替代疗法来根除耐药菌。近期研究者发现外源性CRISPR/Cas9系统能够通过引发不可修复的基因组DNA损伤导致细菌死亡,是一种有前景的抗感染手段。然而,由于缺乏有效的递送载体,CRISPR/Cas9的体内抗菌效力鲜有报道。CRISPR/Cas9质粒具有极大的分子量和电负性,导致体内细菌内化效率过低,无法根除细菌。近日,北京放射医学研究所金义光/袁伯川团队在Journal of Nanobiotechnology(中科院1区,IF: 10.6)上发表了题为“Gene editing tool-loaded biomimetic cationic vesicles with highly efficient bacterial internalization for in vivo eradication of pathogens”的研究论文(2024 22: 787)。研究表明,阳离子脂质杂化的细菌衍生囊泡(biomimetic cationic hybrid vesicles, BCVs)可作为CRISPR/Cas9质粒载体,向病原菌高效递送致死性基因编辑系统,用于根除体内耐药菌,同时验证了载有CRISPR/Cas9质粒的BCVs有望成为治疗耐药细菌感染新型纳米药物。文章的第一作者为贾学丽、袁伯川,通讯作者为金义光、袁伯川。
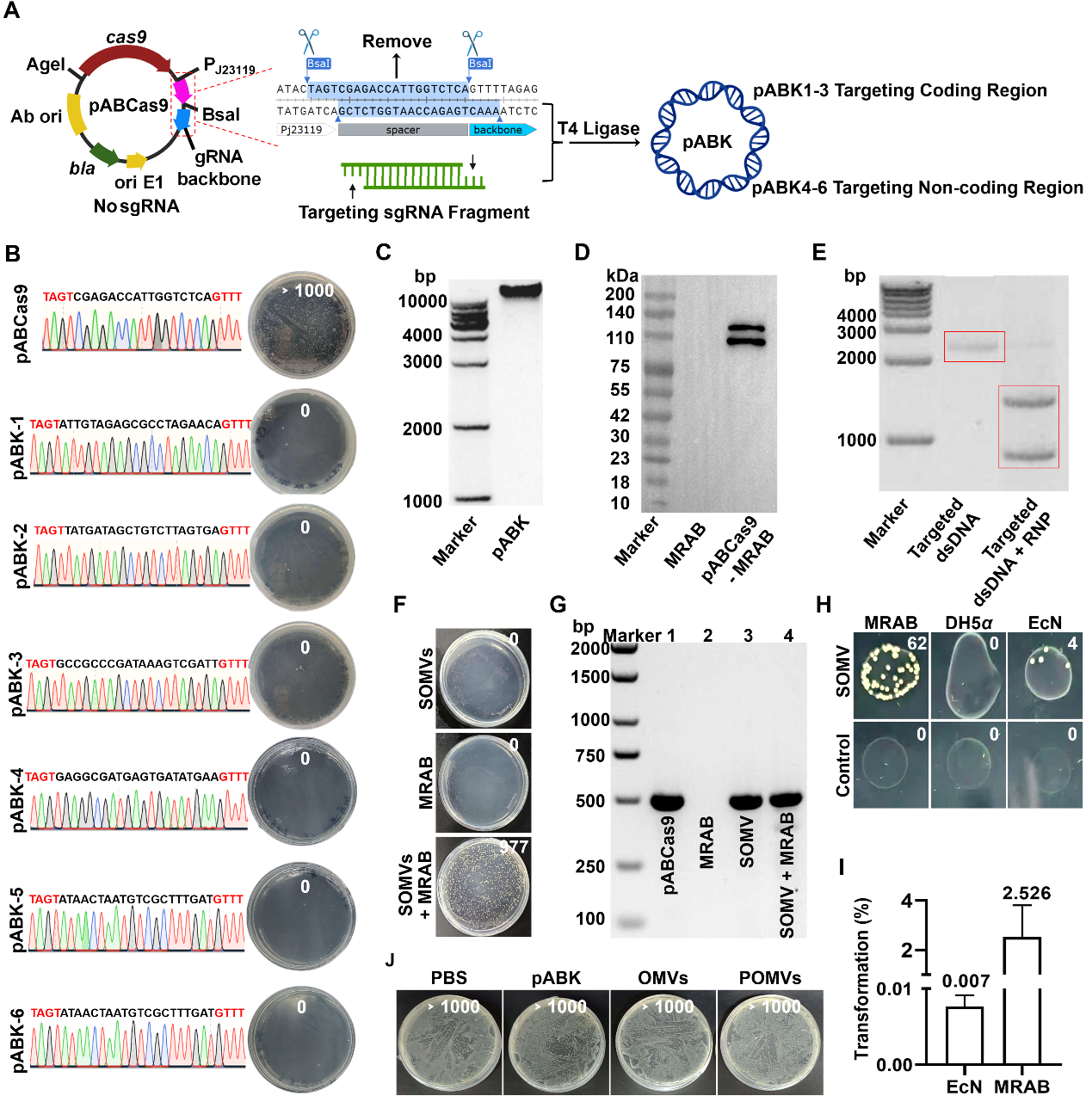
图1 装载CRISPR/Cas9的杂化细菌囊泡治疗耐药菌感染示意图该团队首先构建了靶向MRAB基因组不同位置的CRISPR/Cas9质粒,证明了其在细菌内表达Cas9蛋白和sgRNA并导致DNA双链断裂(DSB),不论靶向基因组编码区、非编码区都能导致细菌死亡且无逃逸现象。随后,证明了含质粒的细菌分泌的外膜囊泡(OMVs)能够介导外源质粒在细菌中水平转移,但是转化率很低不足以产生杀菌效果。
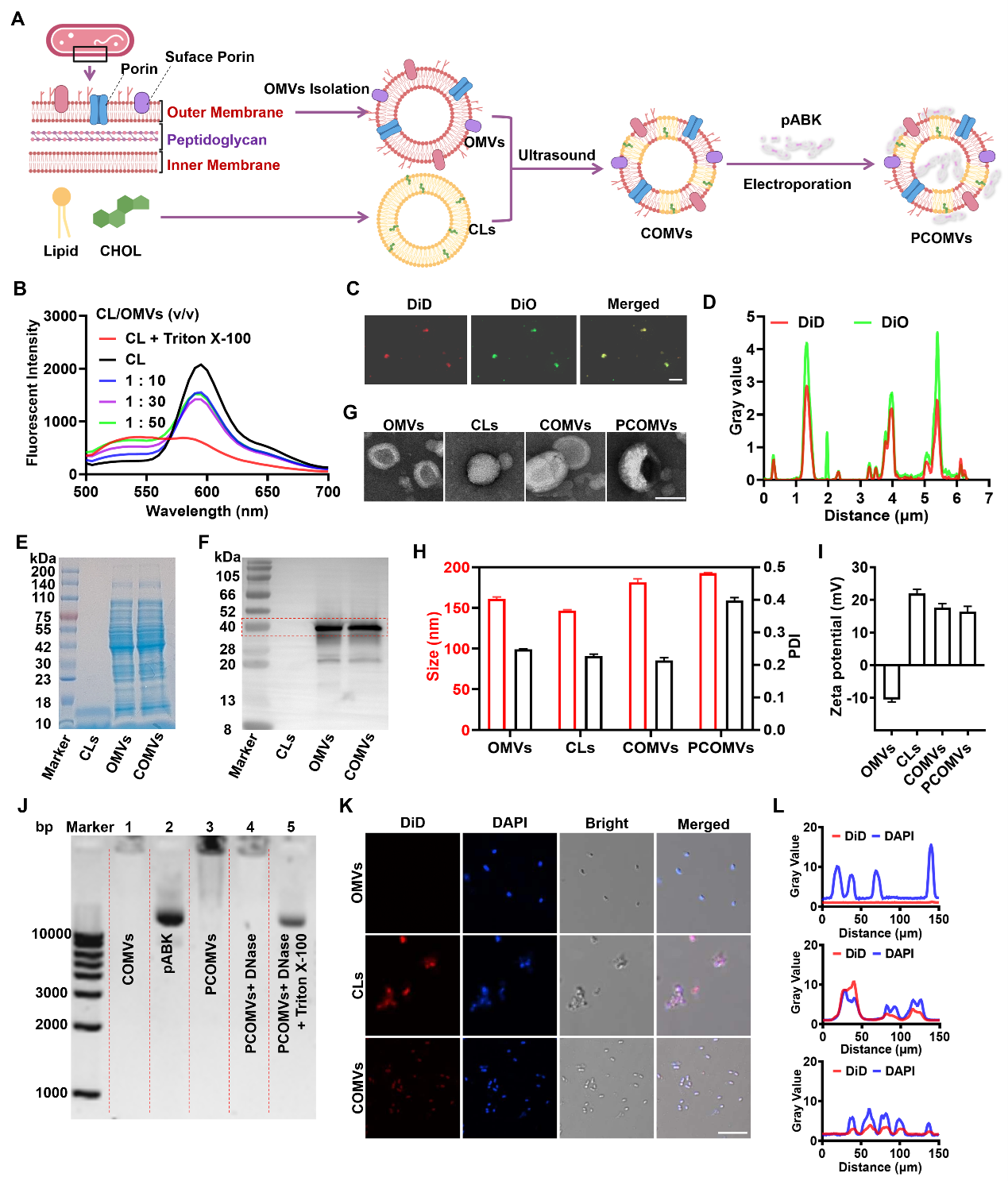
图2 CRISPR/Cas9质粒的抗菌作用与水平转移为了解决OMVs递送效率低的问题,研究人员将阳离子脂质(DDAB)脂质体(CLs)与OMVs杂化以提高递送效果,通过FRET效应、激光共聚焦成像、SDS-PAGE/WB、粒径电位等检测,确定了DDAB与OMVs的均匀杂化形成阳离子杂化囊泡(COMVs)。利用共孵育联合电穿孔的方法将CRISPR质粒装载到杂化囊泡(PCOMVs)上,用DNase处理的琼脂糖凝胶电泳实验证明了质粒既存在于囊泡表面又装载于囊泡内部。激光共聚焦显示COMVs与细菌共孵育后发生了膜融合事件,说明其有效的质粒递送。
图3 COMVs的制备、表征和细菌内化随后,研究者通过体外抗菌实验,摸索了递送效率最优的杂化囊泡制备工艺以及抗菌效果最佳的质粒浓度。通过激光共聚焦和扫描电镜确定了细菌的死亡状态。
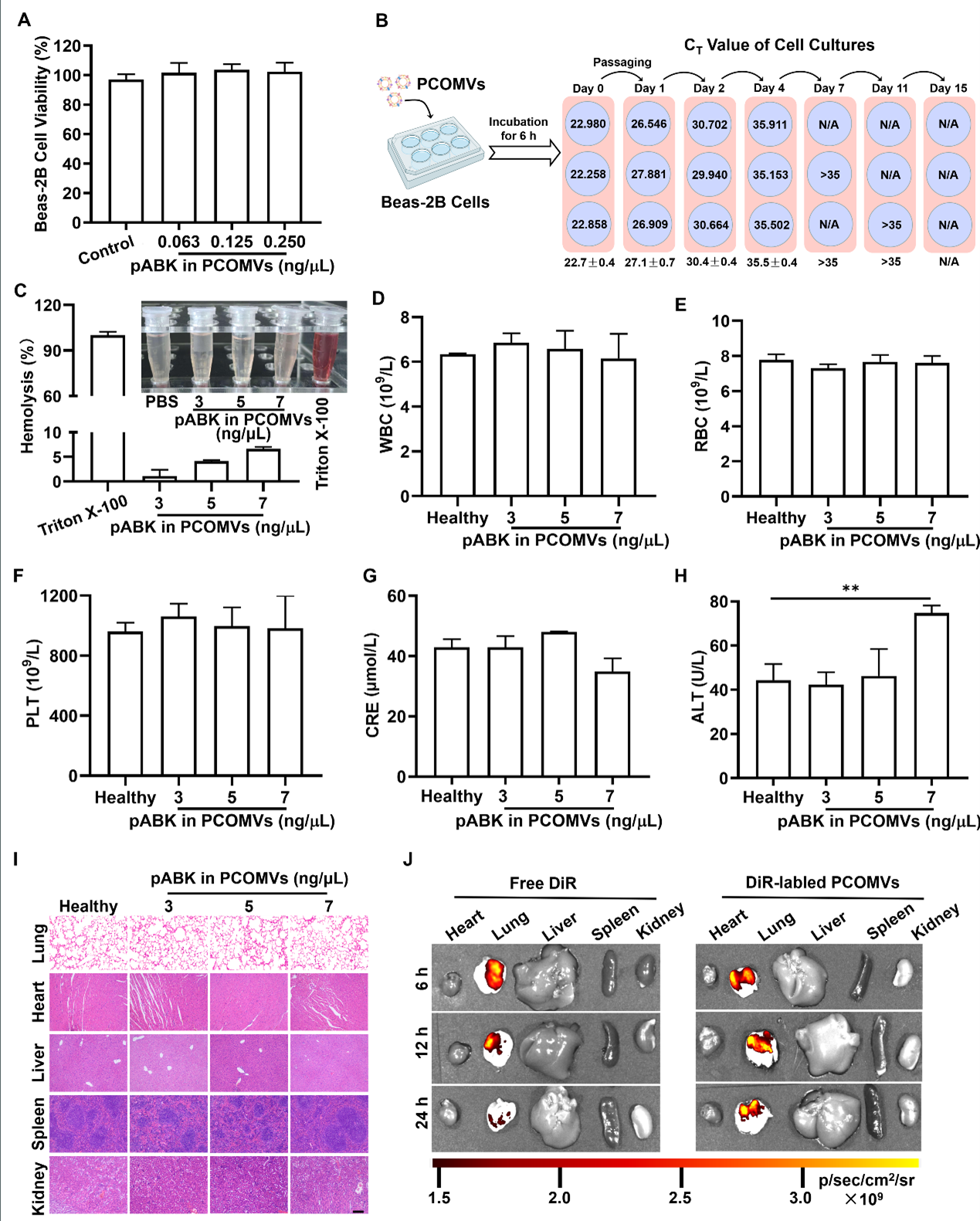
图4 PCOMVs的抗菌效果研究人员进一步验证了PCOMVs的安全性,在使用浓度范围内不会造成细胞死亡,且CRISPR/Cas9质粒由于是细菌特异性的,在哺乳动物细胞内自行清除。PCOMVs的气管给药不会导致严重的白细胞上升、肝肾毒性和主要脏器损伤,且主要分布在肺部各小叶。
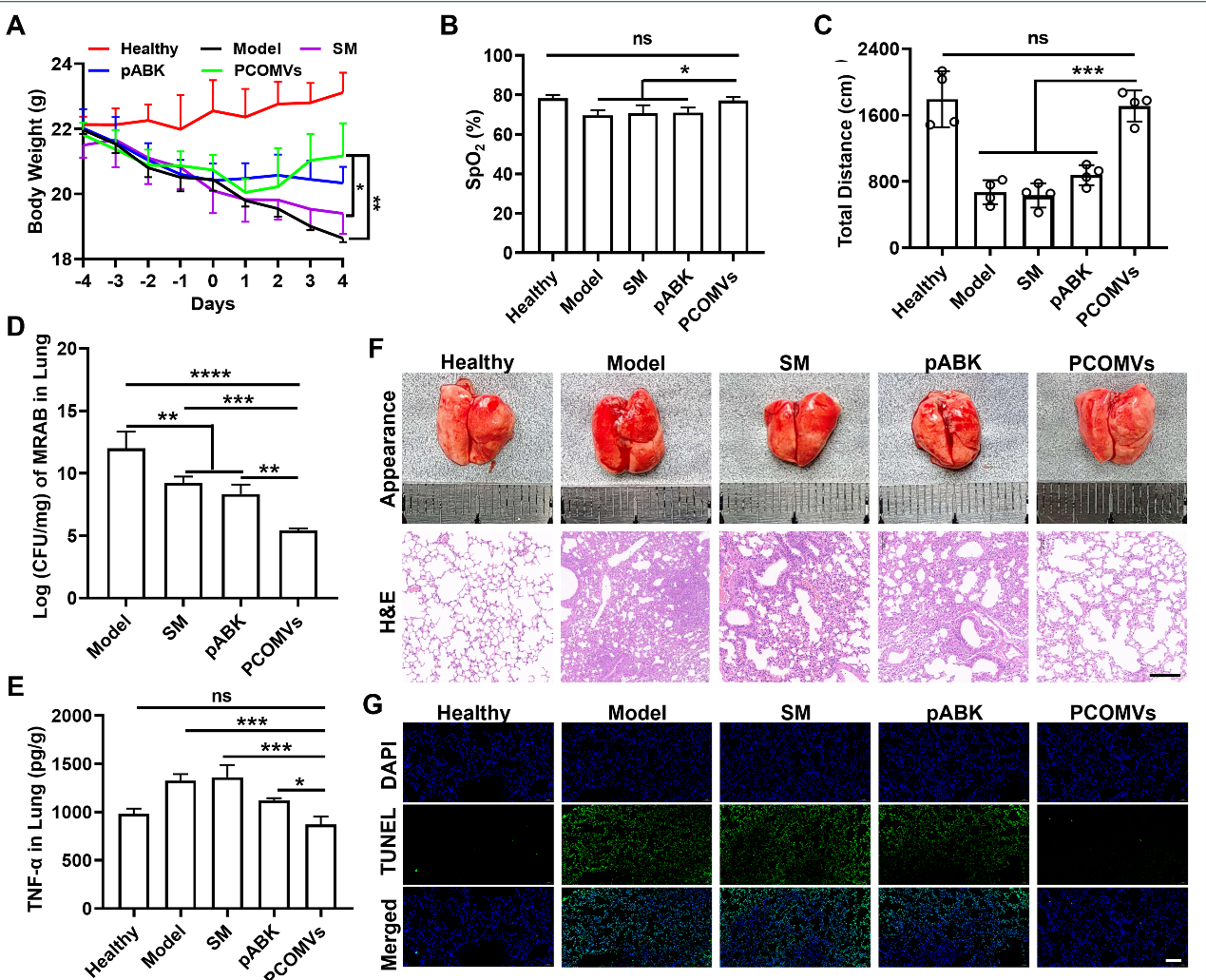
图5 PCOMV的安全性在肺部急性MRAB感染模型中,链霉素的治疗无效,而仅单次气管给药PCOMVs就产生显著疗效,病原菌载荷降低至正常组水平,炎症因子大幅下降,运动能力和肺功能恢复至正常组水平。
图6 PCOMV治疗肺部MRAB感染为了验证BCVs平台递送CRISPR/Cas9质粒抗感染的通用性,研究者制备了铜绿假单胞菌膜囊泡(MVs)与阳离子杂化囊泡(CMVs),同样装载CRISPR/Cas9质粒获得PCMVs。在皮肤DRPA感染模型中,装载PCMVs的空白非抗菌水凝胶产生显著疗效,清除病原菌、加速了感染伤口愈合,并降低炎症因子水平。
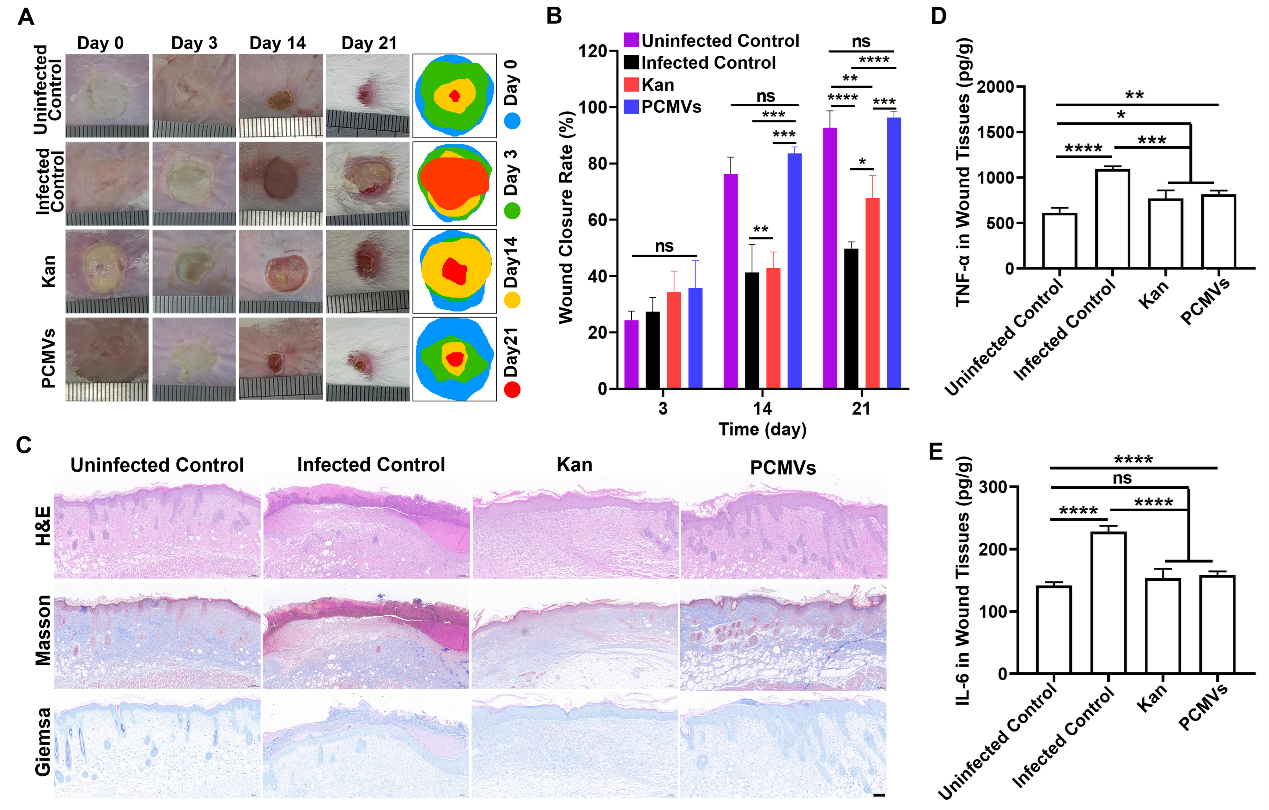
图7 PCMV治疗皮肤DRPA感染这项研究的创新点在于利用仿生阳离子囊泡高效递送CRISPR/Cas9质粒,克服了传统抗生素耐药性的问题。该方法不仅展示了杂化细菌衍生囊泡在治疗耐药性细菌感染方面的巨大潜力,还为未来的抗菌治疗提供了新的思路和工具。装载CRISPR/Cas9的BCVs有望成为治疗耐药性细菌感染的一种有前景的纳米药物。
参考文献:Gene editing tool-loaded biomimetic cationic vesicles with highly efficient bacterial internalization for in vivo eradication of pathogens. J Nanobiotechnol 22, 787 (2024). https://doi.org/10.1186/s12951-024-03065-4.
外泌体资讯网 J Nanobiotechnol│北京放射医学研究所金义光/袁伯川:杂化细菌衍生囊泡装载CRISPR/Cas9系统根除体内耐药菌