肿瘤细胞外泌体是一种由肿瘤细胞分泌的大小在 30 nm -150 nm 之间的细胞外囊泡,携带核酸、蛋白质以及其他生物活性物质。肿瘤细胞外泌体参与了癌症的发生和发展,对肿瘤的早期诊断和治疗具有重要价值。基于外泌体的癌症诊断通常通过检测外泌体核酸、脂质和表面蛋白来实现,因为它们反映了肿瘤类型和进展。
荧光免疫测定是生物检测领域最常用的方法。基于超分辨率荧光显微镜的超分辨率三色荧光共定位(SR-TFC),可以完全排除非特异性结合位点,显著降低假阳性率。在SR-TFC中,金纳米球阵列被用作检测基底。到目前为止,制备纳米阵列免疫基板的两种成熟方法是聚焦离子束(FIB)和电子束光刻(EBL)。FIB能够实现高精度加工和直接蚀刻,但成本高昂,高能离子束也会对样品表面造成损坏。EBL具有高分辨率、灵活性和广泛适用性,但它对工作人员的技术要求很高,需要精确的控制和校准,设备也很复杂。
针对以上问题,东南大学王著元教授团队在Biosensors and Bioelectronics上发表题为“High-precision phenotyping of breast cancer exosomes based on washable magnetic microarrays and super-resolution tricolor fluorescence co-localization”的论文(2025 Feb 11:276:117253),主提出了一种基于 3D 打印技术和磁场控制的 WMMS 制备方法,并利用磁场翻转实现了 WMMS 的可擦洗与可重复利用,提高了 SR-TFC 的实用性。文章第一作者为东南大学博士毕业生魏金秀,通讯作者为东南大学宗慎飞副研究员、东南大学王著元教授。
研究人员应用水热法制备出磁性纳米粒子并对其进行生物功能化修饰。随后,将设计好的结构模型导入 3D 打印系统打印出相应的模板,再利用聚二甲基硅氧烷(PDMS)倒模制备出微纳米孔阵列。最后,通过磁场引导,快速将磁性纳米粒子引入孔中,制备出磁性纳米阵列基底。通过翻转磁场方向,可以将磁性纳米粒子引出微纳米孔阵列,实现微纳米孔阵列的可擦洗和可循环使用。
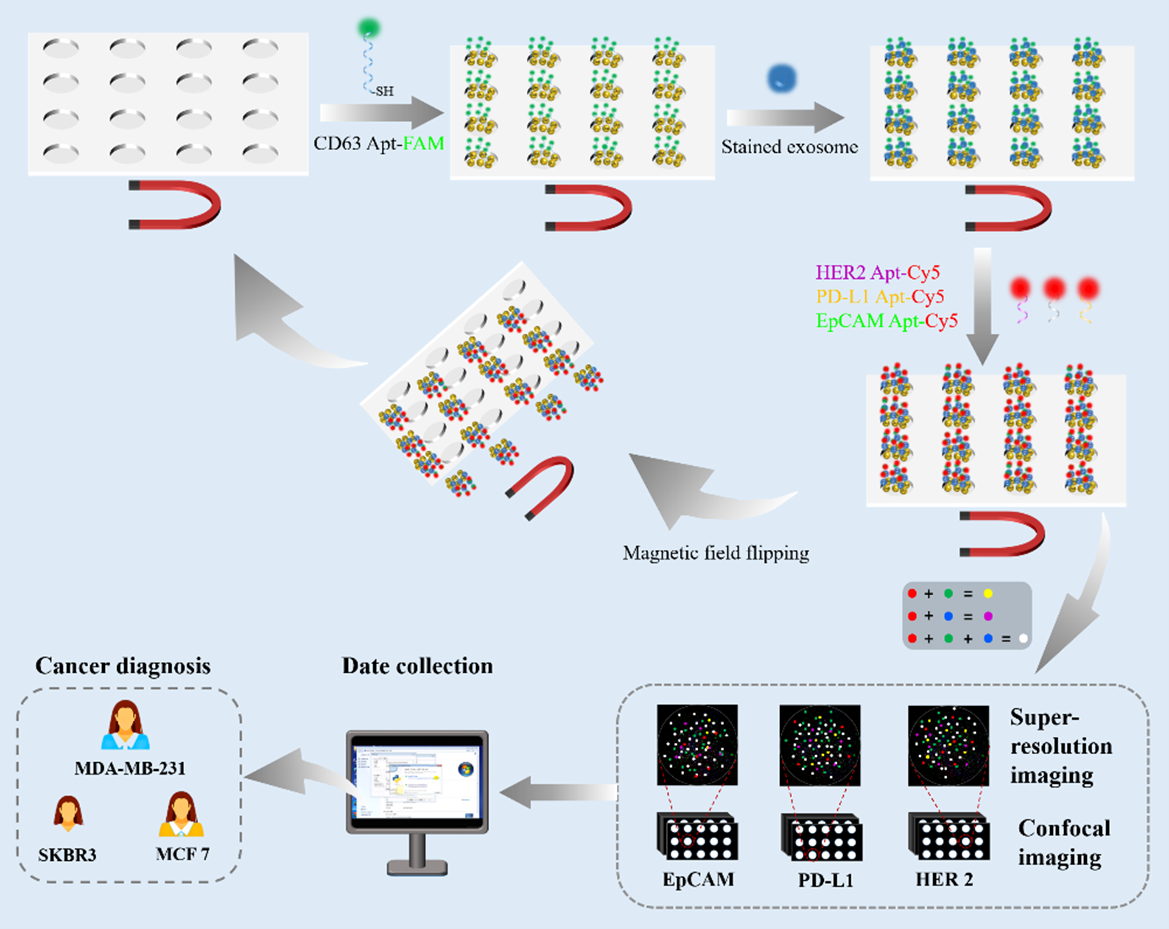
图1 利用WMMS和SR-TFC进行高精度外泌体表型分型的示意图
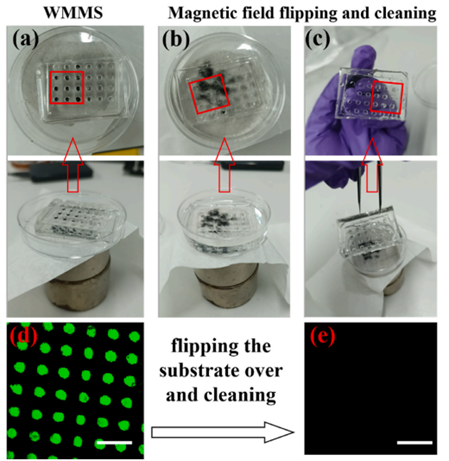
图2 WMMS 的可擦洗性
作为概念验证,以三种乳腺癌亚型细胞的外泌体为例。利用 PD-L1、EpCAM和 HER2 三种蛋白质作为外泌体标志物。通过使用 CFPP 对共定位荧光像素点进行计数,定量分析各种特异性蛋白质,以获得外泌体的 3D 表型信息。
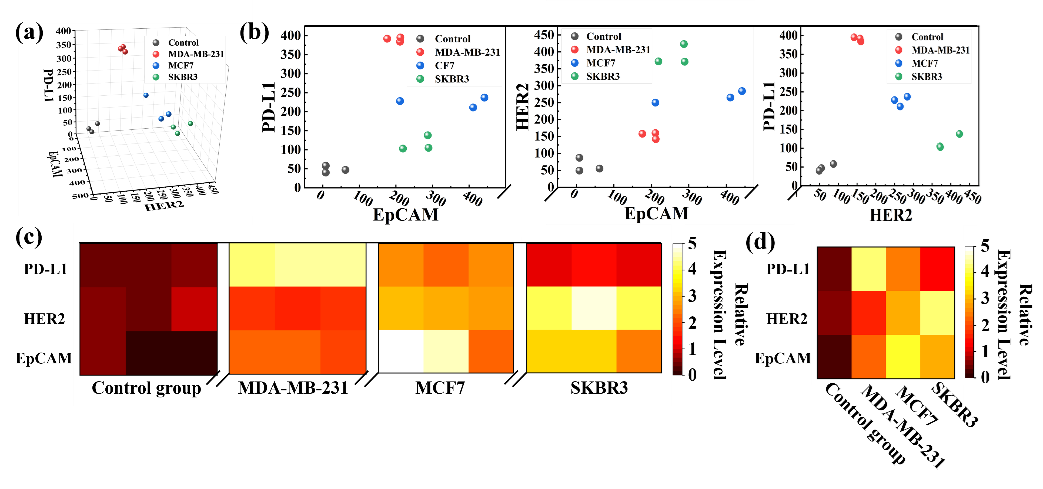
图3通过 CFPP 分析的模拟血清中三种类型外泌体的表型图谱
该方法通过 3D 打印技术和磁场控制快速制备出了 WMMS,简化了基底制备流程,与此同时,该方法亦结合了荧光共定位像素点计数法(CFPP)分析了乳腺癌外泌体上的 PD-L1、HER2 和 EpCAM 三种特异性蛋白质,最大程度地降低检测结果的假阳性率。研究结果表明,通 WMMS-SR-TFC 和 CFPP,能方便可靠地测得外泌体上的 PD-L1、HER2 和 EpCAM 表达水平,提高了 SR-TFC 的实用性,为 SR-TFC 走向实际临床应用打下关键基础。
这项工作得到了中国自然科学基金(NSFC)(62175027,62175030,62305054,62205053)的支持。
参考文献:
High-precision phenotyping of breast cancer exosomes based on washable magnetic microarrays and super-resolution tricolor fluorescence co-localization. Biosensors and Bioelectronics 276 (2025) 117253. https://doi.org/10.1016/j.bios.2025.117253
外泌体资讯网 BIOSENS BIOELECTRON|东南大学王著元:基于可擦洗磁性微阵列基底和SR-TFC 的高精度乳腺癌外泌体表型分析