胃癌是一种常见且具有高度侵袭性的恶性肿瘤,其发病机制尚不明确。然而,外泌体在胃癌的发生发展和治疗中发挥着重要作用。细胞利用外泌体包装和运输多种生物活性分子(如蛋白质、双链DNA和微核糖核酸)至其他位点。外泌体特异性膜结构和外泌体内容物广泛参与促进胃癌细胞间物质交换和细胞间通讯的过程。它们有助于形成转移前微环境,促进胃癌细胞的增殖和凋亡,驱动侵袭、转移和抗肿瘤药物的耐药性。
近期,中国首都医科大学北京友谊医院普通外分中心张军教授、尹杰教授团队联合首都医科大学附属复兴医院尚禹汐教授在International Journal of Biological Sciences上发表题为“Functions and Clinical Applications of Exosomes in Gastric Cancer”的论文,系统总结了外泌体在胃癌发生、转移、耐药及临床诊疗中的关键作用。第一作者为郑智、翟育豪等,通讯作者为尚禹汐、张军和尹杰。
该综述旨在总结截至2024年5月31日在PubMed、Web of Science和Embase数据库检索的关于外泌体在胃癌发病机制中的作用及其在胃癌治疗中的潜在临床应用的研究结果,重点探讨了外泌体在胃癌中的分子机制及临床应用潜力:
- 外泌体与胃癌微环境
- 外泌体通过携带蛋白质(如CD9、HSP70)、核酸(如miRNA、lncRNA)等生物活性分子,参与胃癌细胞增殖、血管生成及转移。例如,胃癌细胞分泌的外泌体可通过传递miR-519a-3p诱导肝转移前微环境的形成(图2)。
- 外泌体通过激活PI3K/Akt、TGF-β/Smad等信号通路,调控肿瘤相关巨噬细胞(TAMs)和癌症相关成纤维细胞(CAFs),促进免疫逃逸和化疗耐药。
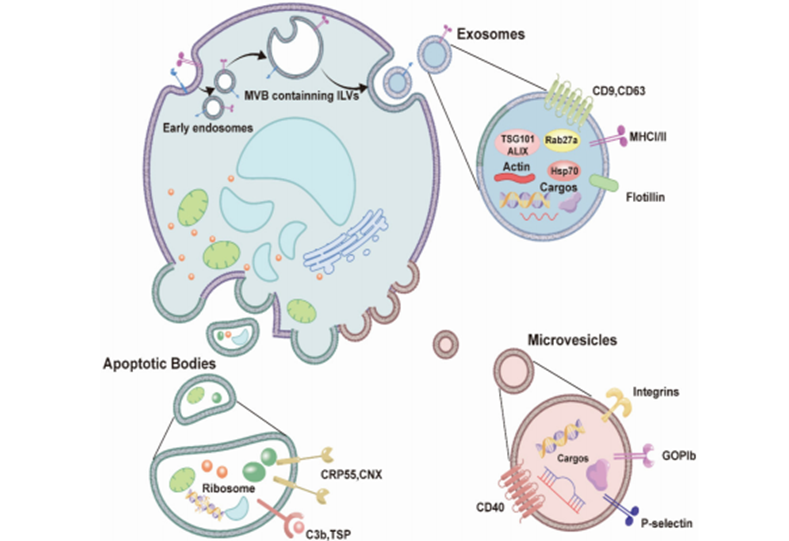
图1:外泌体的生物发生机制,展示细胞内多泡体(MVB)形成、运输及释放过程
- 外泌体作为诊断标志物
- 外泌体中的miRNA(如miR-1246、miR-423-5p)、lncRNA(如lncUECC1)和circRNA(如hsa_circ_0015286)在胃癌患者血清或腹水中显著差异表达,具有高敏感性和特异性。例如,血浆外泌体lncUECC1可区分早期胃癌与健康人群(AUC=0.824)。
- 外泌体表面蛋白(如PD-L1)水平与胃癌预后密切相关,高表达患者生存率较低。
- 外泌体在治疗中的应用
- 外泌体可作为药物载体靶向递送miRNA抑制剂(如抗miR-214)或化疗药物(如5-氟尿嘧啶),逆转耐药性并抑制肿瘤生长。
- 基于外泌体的免疫治疗策略(如靶向PD-1/PD-L1)在临床试验中展现出潜力,但需解决外泌体分离效率低、药物载量有限等技术瓶颈。
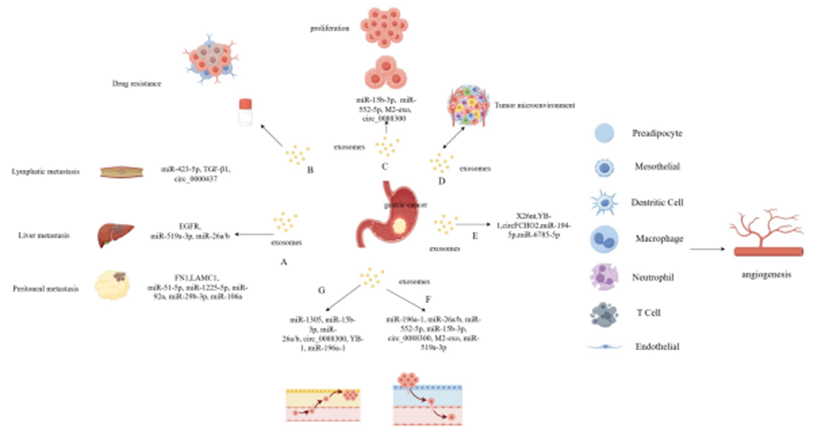
图2:外泌体在胃癌中的调控网络,涵盖血管生成、转移、耐药及微环境重塑等关键环节
二,总结
近年来,外泌体已成为胃癌领域的研究热点,越来越多的研究关注其独特的作用和作用机制。外泌体已被证实在胃癌细胞的生长、增殖和转移中发挥重要作用,部分外泌体可能作为改善早期诊断的生物标志物,或作为药物载体在减少耐药性或促进靶向递送货物的治疗策略中发挥重要作用。虽然外泌体的潜在临床应用很明显,但仍需克服四个主要挑战。首先,外泌体作为胃癌的关键调控分子的作用机制尚不清楚,且既往研究样本量不足阻碍了其临床应用。其次,用于胃癌早期诊断的某些外泌体标志物的表达水平是否存在个体差异,以及特定患者的外泌体标志物的表达水平是否因药物治疗、感染或其他因素而变化,目前仍不清楚。第三,必须进一步提高外泌体内容物的精准高效靶向递送,以优化临床结局。外泌体载体与中药、化合物或单体联合治疗对胃癌患者的影响有待进一步研究。克服上述挑战,进一步探索外泌体在胃癌诊断和治疗中的应用将需要多年的时间。然而,随着科学技术的不断进步和对该领域研究兴趣的不断提高,有望开创一个新的时代,促进胃癌的早期诊断和改善患者预后。
参考文献:
Functions and Clinical Applications of Exosomes in Gastric Cancer, Int J Biol Sci. 2025 Feb 28;21(5):2330-2345. doi: 10.7150/ijbs.98087. eCollection 2025.
外泌体资讯网 Int J Biol Sci|首都医科大学北京友谊医院张军/尹杰/附属复兴医院尚禹汐:胃癌中外泌体的功能及临床应用研究进展





