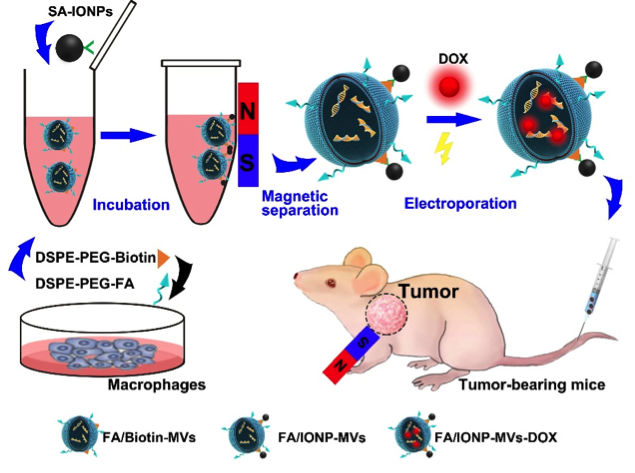
近日,国际纳米研究顶级期刊ACS Nano(IF=13.334)刊登了武汉大学口腔医学院赵怡芳课题组在细胞源性囊泡研究方面的最新研究成果(Magnetic and Folate Functionalization Enables Rapid Isolation and Enhanced Tumor-Targeting of Cell-Derived Microvesicles)。他们利用磷脂衍生物“自然嵌合”的策略获得膜生物素化和叶酸化的细胞源性囊泡,再用亲和素修饰的磁性纳米颗粒通过亲合作用实现对细胞源性囊泡的磁性修饰,实现了囊泡的高效磁分离,更重要的是磁/叶酸双重靶向极大的提高的了囊泡的肿瘤靶向性,在裸鼠肿瘤模型中取得了较好的肿瘤靶向治疗效果。
细胞源性囊泡(MVs)是细胞膜出芽、脱落产生的囊性结构,是细胞间传递生物大分子的天然载体。鉴于其天然的运载属性和良好的生物安全性,细胞源性囊泡被认为是极具前景的药物运载平台,也是近年来肿瘤药物运载领域的研究热点。然而,细胞源性囊泡的获取依赖于超高速离心,该方法繁琐、耗时,且受限于昂贵的超高速离心设备。因此,限制细胞囊泡其在临床治疗中的大规模应用。此外,细胞源性囊泡本身靶向肿瘤的能力较弱,难以在肿瘤部位选择性富集。利用赵怡芳课题组先前发明的 “生物膜磷脂嵌合”策略,他们提出了一种新的细胞囊泡分离、富集和靶向修饰的方法。首先,收集经生物素化的巨噬细胞的培养上清;然后,利用链霉亲和素偶联的磁性纳颗粒(SA-IONPs)与细胞囊性囊泡表面生物素的特异性结合,在外界磁场作用下,将细胞源性囊泡自培养上清中分离、富集,从而得到纳米磁颗粒和叶酸双重修饰的细胞源性囊泡。该囊泡具有极强的靶向肿瘤的能力,将抗肿瘤药物载入后,可发挥强有力的肿瘤杀伤效应。总之,本研究提供了一种新的细胞囊泡分离、富集和靶向修饰的方法,实现了对细胞源性囊泡的大规模、快速、简便的分离和制备,并同时赋予这些天然载体良好的肿瘤靶向性,极大推动了细胞源性囊泡作为药物载体在肿瘤治疗领域的应用。
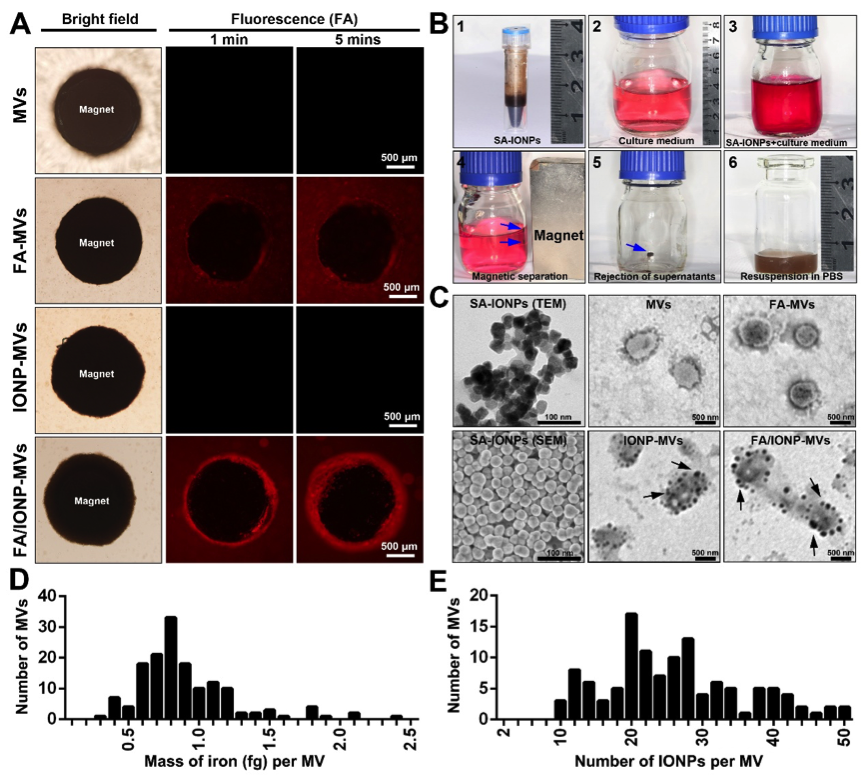
图2. 磁/叶酸修饰的囊泡的磁性分离。
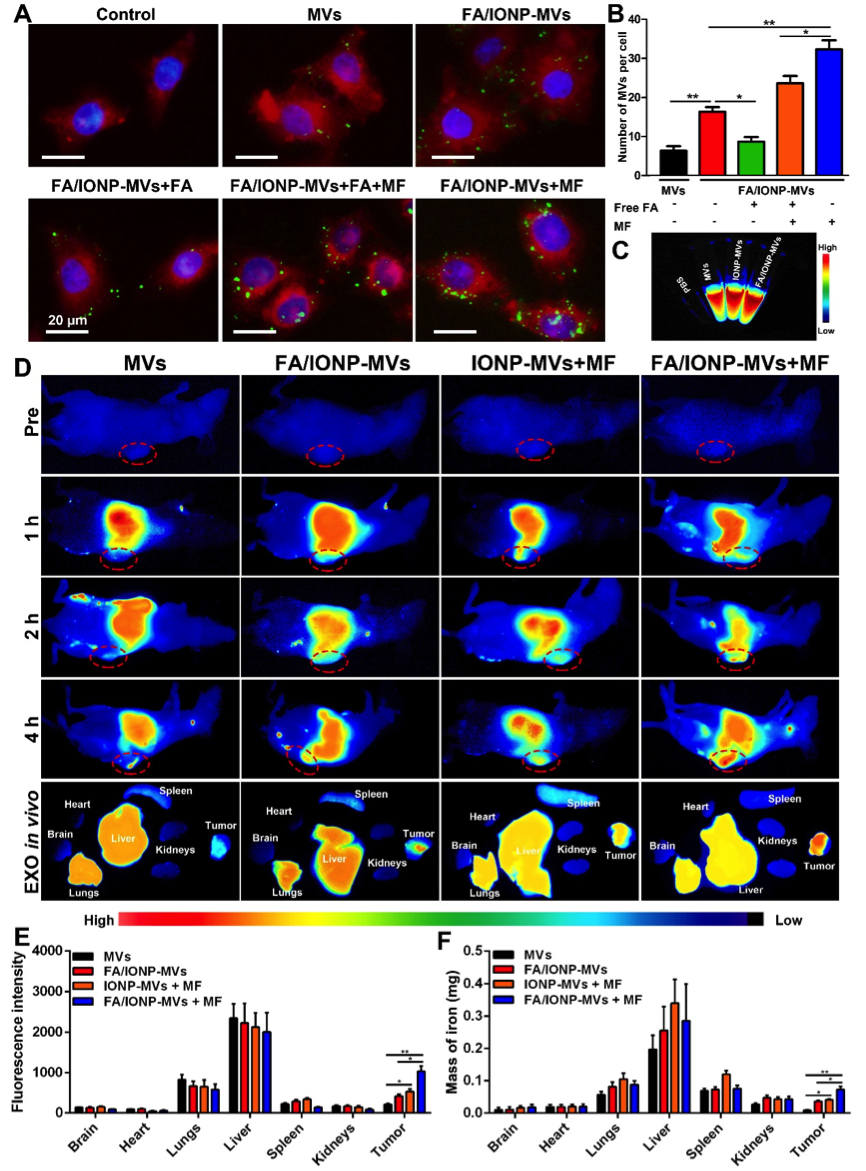
图4. 磁/叶酸修饰的囊泡具有较强的肿瘤靶向性。
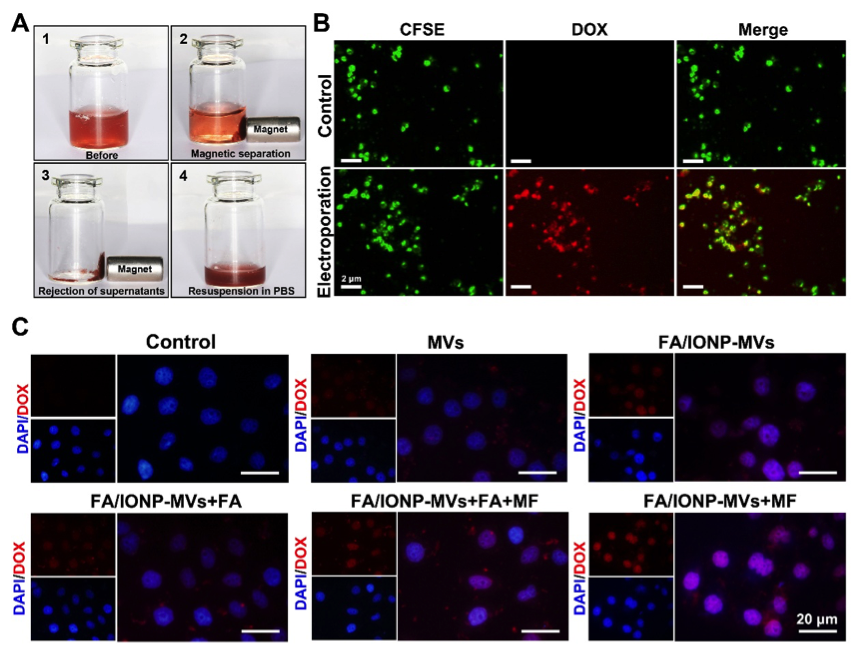
图5. DOX装载与细胞内释放。
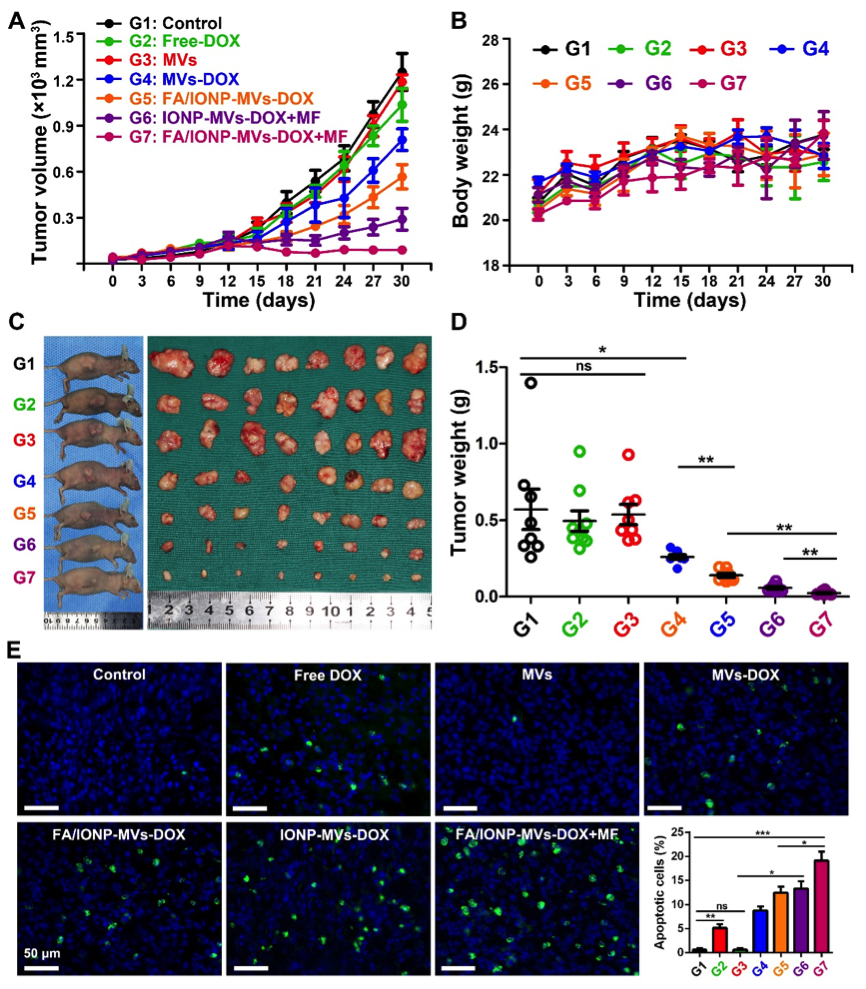
图6. 磁/叶酸修饰的囊泡作为肿瘤靶向治疗的载体。
参考文献:Wei Zhang1, Zi-Li Yu1, Min Wu, Jian-Gang Ren, Hou-Fu Xia, GuoLiang Sa, Jun-Yi Zhu, Dai-Wen Pang, Yi-Fang Zhao, and Gang Chen, Magnetic and Folate Functionalization Enables Rapid Isolation and Enhanced Tumor-Targeting of Cell-Derived Microvesicles, ACS Nano, 22 Dec 2016.
>>>原文链接:http://pubs.acs.org/doi/abs/10.1021/acsnano.6b05630.
版权归外泌体之家和原作者所有,欢迎转载,但请注明出处和原文链接!
原文下载和讨论请点击:http://www.exosome.com.cn/thread-1340-1-1.html?_dsign=740291ec