前列腺癌是全世界男性最常见的癌症之一。在四分之三的前列腺癌患者中,会出现癌症转移,原位肿瘤会扩散到体内的远端部位。转移性前列腺癌细胞经常会转移到骨骼,影响骨骼结构并导致严重的疼痛、病理性骨折和脊髓压迫。所以,如果能更好地理解这些癌细胞影响骨骼的过程可能有助于寻找新的治疗方法。在美国国家科学院院刊PNAS上发表的一项研究中,东京医科和牙科大学(TMDU)的研究人员报告了一种RNA分子,该分子可能在前列腺癌引起的骨重建中起关键作用。
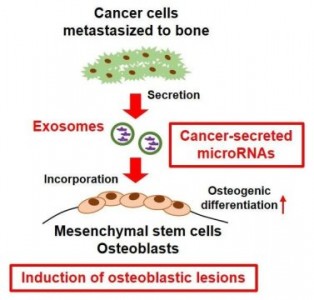
图:在骨转移性微环境中,转移的癌细胞与周围骨细胞之间的联系对于成骨细胞形成或溶骨性表型是关键的。miRNA通过外泌体在细胞间转移并影响其受体细胞的表型。本研究表明癌症分泌的,miRNA通过促进成骨细胞的成骨分化诱导肿瘤骨转移。
通过骨形成(成骨细胞)和骨吸收(破骨细胞)两种细胞的良好平衡维持了正常的骨发育过程。转移至骨的肿瘤细胞改变这些细胞的活性,改变程度取决于癌症的类型,肿瘤细胞引起成骨细胞改变或溶骨性改变。
“转移性肿瘤细胞可促进骨形成或骨吸收,”第一作者Kyoko Hashimoto解释说。 “成骨细胞损伤是在前列腺癌中常见的骨形成部位,这些损伤会导致骨骼结构薄弱,甚至更糟,会促进肿瘤的生长,如果我们能够弄清楚前列腺癌细胞如何改变骨骼内部的环境来诱导成骨细胞破坏的过程中,我们就可以找到新的治疗靶点。“
为了做到这一点,研究人员寻找促骨形成的前列腺癌细胞与促骨吸收的乳腺癌细胞的差异。研究人员专注于microRNA这个调节各种基因表达的分子。最近的研究表明,microRNA通过外泌体从细胞递送到其他细胞以充当细胞间通讯工具。癌细胞分泌的miRNA可改变非癌细胞中的基因表达,破坏其正常功能并促进肿瘤生长。
研究人员检测了一组microRNA,并比较了它们在前列腺癌和乳腺癌来源的外泌体中的丰度。其中,特别是miR-940在前列腺癌衍生的外泌体中高度丰富,并且在促进骨形成中起到强大的作用。
Hashimoto补充说:“我们发现miR-940可以从转移性癌细胞中分泌出来,并改变存在于骨骼中其他细胞的基因表达,从而使它们具有成骨细胞样的特性。当把肿瘤植入胫骨或小鼠头骨时,我们发现表达miR-940的肿瘤细胞可以诱发典型的前列腺癌的成骨细胞性病变。”
引人注目的是,当miR-940在促骨吸收的乳腺癌细胞中表达时,这些细胞引发了小鼠骨形成损伤,就如同前列腺癌细胞中的结果类似。研究结果表明,miR-940在前列腺癌的骨形成能力中起着核心作用。
“我们的研究表明microRNAs是调节骨重塑并促进转移性前列腺癌肿瘤生长的重要因素,”研究人员Shingo Sato总结说,“一旦癌症已经转移到骨骼上,通常是无法治愈的,所以对转移过程的任何了解都对于寻找新的治疗方法是非常有用的。我们希望我们的研究结果最终将为这种形式的治疗靶点开辟新的途径癌症。”
参考资料:
1. Kyoko Hashimoto, Hiroki Ochi, Satoko Sunamura, Nobuyoshi Kosaka, Yo Mabuchi, Toru Fukuda, Kenta Yao, Hiroaki Kanda, Keisuke Ae, Atsushi Okawa, Chihiro Akazawa, Takahiro Ochiya, Mitsuru Futakuchi, Shu Takeda, Shingo Sato. Cancer-secreted hsa-miR-940 induces an osteoblastic phenotype in the bone metastatic microenvironment via targeting ARHGAP1 and FAM134A. Proceedings of the National Academy of Sciences, 2018; 115 (9): 2204
2. "Forming and resorbing bones: metastasizing cancer cells modify bone remodeling with small RNA secretion." http://www.tmd.ac.jp/english/press-release/20180319_1/index.html
3. "Metastatic cancer cells modify bone remodeling with small RNA secretion in bone metastasis." https://www.sciencedaily.com/releases/2018/03/180323104831.html