长链非编码RNA(lncRNA)以及外泌体在肿瘤生物学中起着重要的调节或交流作用。然而,外泌体lncRNAs在胰腺导管腺癌(PDAC)肿瘤侵袭或转移中的作用和机制仍然未知。来自陆军军医大学西南医院李晓武课题组的研究人员在Oncogene杂志发表文章,证实胰腺癌lncRNA Sox2ot可以在肿瘤侵袭或转移中发挥作用,深入探究了其在PDAC中相应的详细分子机制,并提出了一个关于肿瘤来源的外泌体lncRNA如何促进PDAC中肿瘤侵袭和转移的系统性假说。
胰腺导管腺癌(PDAC)是最具侵袭性的癌症之一,中位生存时间少于6个月,5年生存率低于5%。不良预后部分归因于PDAC表现出早期侵袭和快速转移。研究表明肿瘤转移是涉及许多致癌因素的多步骤过程。上皮-间质转化(EMT)在肿瘤细胞侵袭的早期阶段显示出至关重要的作用。肿瘤干细胞也具有“播种”新肿瘤的能力。研究PDAC的详细转移机制可能有助于鉴定新的诊断分子标记物或治疗靶标。
长链非编码RNA(lncRNA)是一类长度超过200个核苷酸的转录RNA,不具有编码蛋白质的能力,但最近被鉴定为转录和表观遗传网络的新调控因子。作为染色质相关介质或竞争性内源RNA,越来越多的lncRNAs表现出异常表达,并在许多肿瘤中发挥重要作用。许多肿瘤生物学行为,如细胞凋亡、侵袭或转移,都归因于不同的lncRNAs的作用。最近的研究表明,lncRNAs可以与miRNAs相互作用形成侵袭性或转移性级联系统。然而,PDAC中转移相关的lncRNAs检测并不完全,需要进一步被研究。
外泌体是胞内体衍生的小囊泡,直径范围从30到100nm。虽然外泌体首先在红细胞中被发现,但大量研究表明外泌体也可以被不同类型的肿瘤细胞分泌。外泌体可携带大量的RNA或蛋白质,通过细胞间通讯的方式将遗传或蛋白质组信息转移至受体细胞。研究表明,肿瘤细胞可以将外泌体分泌到基质细胞中以重新编程肿瘤微环境的细胞,促进肿瘤的侵袭或转移。目前,已经鉴定出许多外泌体miRNA或蛋白质能够促进肿瘤进展。在PDAC中,外泌体来源蛋白MIF可以诱导肝脏转移前的微环境的形成并增强肝脏转移。然而,lncRNA在PDAC肿瘤来源的外泌体中的作用仍然未知。
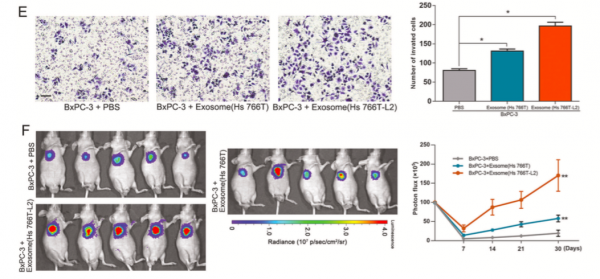
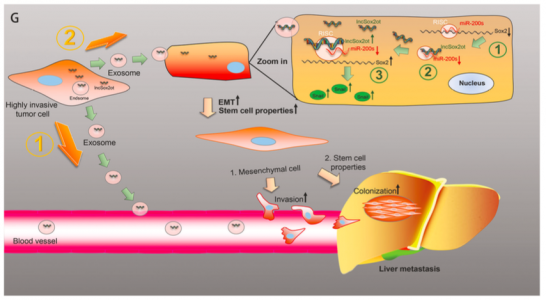
在这项研究中,研究人员探讨了肿瘤来源的外泌体在PDAC进展和转移中的体外和体内的详细作用和机制。研究人员从高侵袭性PDAC细胞的外泌体中鉴定了lncRNA-Sox2ot,并且分析了血浆样品中Sox2ot的表达,发现血浆外泌体里Sox2ot的高表达且与PDAC患者的TNM分期和总生存率相关。进一步的研究表明,Sox2ot通过调节Sox2表达来促进上皮-间质转化(EMT)和干细胞样性质。 Sox2ot竞争性结合miR-200家族来调节Sox2的表达,从而促进PDAC的侵袭和转移。研究人员还证实了外泌体从PDAC细胞向受体PDAC细胞的传递,外泌体Sox2ot可以在体外和体内促进肿瘤侵袭和转移。进一步研究证实肿瘤产生的外泌体可以在体内条件下的肿瘤细胞或血液循环中分泌。最后,研究人员观察到PDAC患者术后血样中外泌体Sox2ot的表达降低。 exosomal lncRNA Sox2ot在肿瘤进展中起重要作用,并且可能是胰腺癌预后的预测标志物。
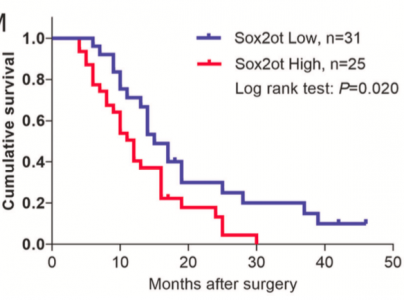
图2: PDAC患者血液Sox2ot的表达与预后相关。
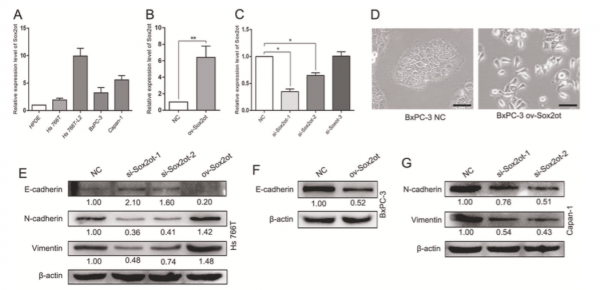
图3: Sox2ot促进PDAC的EMT和肿瘤干细胞特性
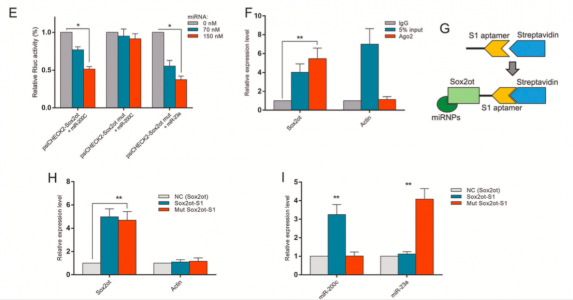
图4: Sox2ot与miRNA-200竞争性作用调节其靶点Sox2
参考文献:Li Z, Jiang P, Li J, Peng M, Zhao X, Zhang X, Chen K, Zhang Y, Liu H, Gan L,
Bi H, Zhen P, Zhu J, Li X. Tumor-derived exosomal lnc-Sox2ot promotes EMT and
stemness by acting as a ceRNA in pancreatic ductal adenocarcinoma. Oncogene. 2018
Apr 12. doi: 10.1038/s41388-018-0237-9.