作者:企鹅
公司们希望使用囊泡包装小分子、蛋白质和RNA药物,甚至将它们本身用作治疗。
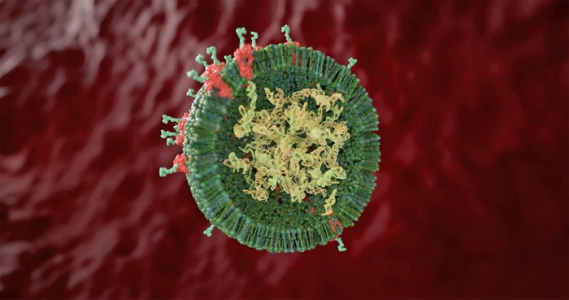
生物技术公司希望使用外泌体来递送多种类型的分子,包括核酸。如上图横截面所示。
数以百万计的细小膜泡从细胞中释放出来并携带各种分子,现在正在通过你的血液流动。直到最近,只有少数研究人员在专注这种小囊泡。
Stephen J. Gould是这些科学家之一。十多年来,Gould花费了大量的时间和资源来研究令人好奇的细胞信使。这些脂质囊泡称为外泌体,可以在相邻和远端细胞之间传递蛋白质和遗传信息。“它们只是我们生物学中无处不在的事实,”这位约翰霍普金斯大学医学院教授说。
现在,它们已成为药物输送的工具。
几十年来,科学家已经了解了外泌体。2006年,PubMed中只有508篇文章被提到了它们。 今天,该网站的搜索带来了超过8,000次点击,其中包括过去一年的几个高质量出版物。
该研究领域火起来部分归因于哥德堡大学的瑞典科学家Jan Lötvall。外泌体长期以来被视为仅仅是从细胞中抛出的微小垃圾囊,但Lötvall在2007年研究表明,一些细胞相互之间使用外泌体转移遗传物质——信使RNA,使蛋白质和microRNAs调节基因的表达(Nat.Cell Biol.2007,DOI:10.1038/ncb1596)。这一发现让科学家们意识到外泌体可能参与健康和疾病病理生理过程,甚至可以利用外泌体作为治疗方法。
“一开始业界对此存在巨大的怀疑态度,而且现在还有一些,”Lötvall说。
图片来源: Evox Therapeutics
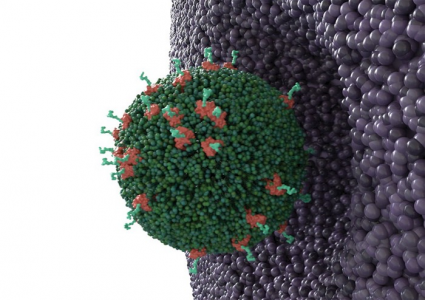
外泌体可以将治疗药物传递给难以触及到的细胞。
Lötvall的研究是里程碑式的。囊泡参与疾病的发生发展,包括癌症和代谢病症,如糖尿病和肥胖症。最近的一项研究甚至指出,外泌体是分泌淀粉样蛋白β的罪魁祸首,淀粉样蛋白β是一种在阿尔茨海默病患者大脑中积聚的斑块形成蛋白。如果外泌体可以如此容易地携带传播疾病的分子,科学家们开始认为它们可能对阻止疾病进展有用。
“Lötvall改变了人们对外泌体的看法,”Codiak BioSciences首席执行官Doug Williams说。 “很明显,这是一个非常重要和古老的信使系统。”
Codiak是越来越多的生物技术初创公司之一,他们试图劫持信使系统,将药物运送到身体某些部位的细胞中。Codiak是投资者的宠儿,自2016年以来筹集了近1.7亿美元,但在过去的几年里,还有十多家公司也开始研究基于外泌体的疗法。有些公司是由同行评审的研究支持的;也有些公司被怀疑是兜售外泌体作为万灵药。
像Codiak一样,许多人正在操纵外泌体来解决一系列令人眼花缭乱的治疗药物传递问题:小分子、RNA疗法、蛋白质、病毒基因疗法,甚至是CRISPR基因编辑工具。细胞和动物的研究表明,这些成分外泌体都可以包装。
还有一些人正在利用外泌体本身,当源自干细胞时,可能成为再生医学的新分支。几家公司已经说服大型制药公司使用他们的技术。
对于Gould来说,突如其来的兴趣令人震惊。就在两年前,“人们会说我们非常接近了解生物学,但离治疗和诊断还很遥远,”他说。然而,基于外泌体的癌症诊断已经可用,并且多种外泌体疗法可以在明年的临床试验中开始测试。
药物载体
Williams记得2011年他加入制药公司担任研发副总裁后不久就和他的Biogen同事一起聊聊了外泌体。牛津大学Matthew J. A. Wood小组的一项研究,其令人震惊的证据表明外泌体携带小干扰RNA(siRNA)可以到达小鼠脑内的细胞(Nat.Biotechnol。2011,DOI:10.1038 / nbt.1807)。一旦超过大脑的保护屏障,遗传物质就会降低BACE1的产生,BACE1是一种参与阿尔茨海默病的蛋白质。Williams说:“我对这个概念很感兴趣,但我们从未在Biogen开展过这方面事情。”
然后在2015年,在访问德克萨斯大学MD安德森癌症中心期间,Williams了解了癌症生物学家Raghu Kalluri和Valerie LeBleu实验室正在进行的工作。他们使用外泌体成功地将siRNA疗法传递给小鼠的癌细胞。
这项研究有可能克服科学家们十多年来一直在努力解决的问题:让siRNA进入正确的细胞。合成脂质纳米粒子已成为siRNA和其他RNA疗法的主要递送装置,但它们可在人体内引起毒性免疫应答。多年来,尽管他们的设计已经有所改善,但它们仍然因在肝脏中聚集而臭名昭着,这限制了制药商能够有效针对的疾病种类。
Kalluri的数据显示,虽然许多外泌体也聚集在肝脏中,但是大量的外泌体也能够前往其他器官,包括胰腺。他的团队使用它们来递送siRNA,这种siRNA阻止了一种叫做KRas的突变蛋白的产生,这是最“不可挽回的”癌症靶点之一。
静脉注射Kalluri的载有siRNA的外泌体可以比载有siRNA的脂质纳米颗粒的类似注射更好地抑制小鼠的胰腺癌,并且没有任何明显的免疫反应(Nature 2017,DOI:10.1038 / nature22341)。“这对我来说是个重要时刻,” Williams回忆道。
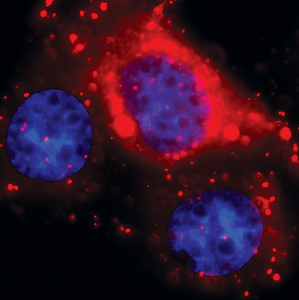
图片来源: Kathleen Marie McAndrews
MD安德森癌症中心的科学家证明,外泌体(红色)可以在人胰腺癌细胞(蓝色)中积聚,释放出抗癌药物。
Kalluri与麻省理工学院和哈佛大学Broad研究所的Eric Lander联合创办Codiak,Williams离开Biogen成为初创公司的首席执行官。Codiak现在推进其自己的KRas计划以及使用外泌体递送小分子和多肽的其他计划。“似乎所有的细胞都会产生外泌体,所有的细胞都可以吸收它们,” Williams说。“外泌体适用于每个治疗领域。”
MD安德森的LeBleu希望癌症中心今年开始进行临床试验,对她和Kalluri的胰腺癌治疗进行测试。他们实验室的装载了siRNA的外泌体,还可以追踪其它的靶标。“我们可能已经找到了一种可以彻底改变无法成药(undruggable)方法的工具,”她说。
其他公司也在蓬勃发展。“该领域正在大规模扩张,”Evox Therapeutics公司首席执行官Antonin de Fougerolles表示。该公司由牛津大学教授Wood共同创办,他使用外泌体将siRNA转入小鼠大脑。Evox正在开发基于外泌体的罕见疾病治疗方法,特别是需要进入大脑的疾病。这家初创公司已经与德国巨头Boehringer Ingelheim和第二家未透露的制药公司建立了合作伙伴关系。
另一家初创公司Anjarium Biosciences正在创造所谓的杂交体,合成脂质纳米粒和天然外泌体的混搭。马萨诸塞州综合医院的Casey Maguire领导的一个小组已经在外泌体中包装了一个腺相关病毒基因治疗——他称这个组合为一个病毒体(vexosome)——将病毒转运到通常很难到达的细胞中,例如内耳感觉细胞。(Mol.Ther.2016,DOI:10.1016 / j.ymthe.2016.12.010)。另一个研究小组最近使用微囊泡——外泌体的“表亲”——将蛋白质、mRNA和CRISPR/Cas9基因编辑系统递送到细胞中(Nat.Commun.12012,DOI:10.1038 / s41467-018-03390-x)。
外泌体本身用于治疗
除了工程外,如果外泌体被证明是有效的药物递送载体,它们的成功可能源于它们与人体的相容性。这就是为什么几个团队正在寻找天然外泌体的替代来源。还有很多其他人认为外泌体本身会治疗许多疾病。
Stella Kourembanas和S. Alex Mitsialis没有想着成为外泌体专家。这两位波士顿儿童医院的科学家花费了十多年的时间,试图挖掘干细胞的潜力,为肺部严重受损的新生儿创造再生疗法。他们的团队证明,人类间充质干细胞(MSCs)——可以转化为多种细胞的成体干细胞——可以通过减少炎症和修复肺组织来治疗肺病动物模型。
他们的第一个猜测是,MSCs通过与受损组织融合并成为肺细胞而起作用。 但仔细观察发现供体干细胞没有驻留。“这是一个悖论,”Mitsialis说。
这导致团队长达数年的时间来解释细胞的再生特性。2012年,研究人员最终表明,MSCs释放的细胞外囊泡可预防小鼠肺损伤。然后该小组花了几年时间学习如何从干细胞中分离和纯化外泌体。去年,他们发现MSC衍生的外泌体对治疗患有严重肺病的小鼠有治愈效果(Am. J. Respir. Crit. Care Med.2017,DOI:10.1164 / rccm.201705-0925oc)。
现在,该团队正在与美国食品和药物管理局以及一个未公开的行业合作伙伴进行谈判,以便在新生婴儿中使用外泌体来治疗同样的疾病,称为支气管肺发育不良,其患病率随着早产儿存活率的增加而增加。
“美国食品和药物管理局希望确保我们治疗风险最高的最严重的婴儿,”Kourembanas说道,他也是波士顿儿童医院新生医学部门的负责人。“我认为急于将干细胞送入诊所时,有许多步骤没有得到仔细考虑,”她说。“我们不能用外泌体重复这一点。”
在许多情况下,尚不清楚外泌体内的哪些分子具有治疗特性,但是几个干细胞公司仍在转向外泌体。例如,Capricor Therapeutics,成立于2005年,开发源自心脏组织的干细胞疗法,现在使用来自相同细胞的外泌体试图治疗心脏和炎症。Capricor与美国陆军合作,用外泌体治疗野外创伤相关疾病。
ArunA Biomedical成立于2003年,最近在中风的啮齿动物和猪模型中测试了源自人类MSCs和神经干细胞的外泌体。该公司报告改善了动物脑细胞和运动神经(Stroke 2018,DOI:10.1161 / strokeaha.117.020353)。ArunA首席执行官Steven Stice说,到2020年,该项目的外泌体临床试验可以开始。
还有一些公司采取不那么谨慎的方法,放弃传统的临床试验和FDA批准,直接面向消费者。通常是那些流氓干细胞治疗诊所,这些公司正在诱使客户提出未经证实的声明,表明外泌体可以帮助美容、勃起功能障碍、免疫疗法、整形外科等。
虽然干细胞在动物研究中表现出奇迹,但在人类身上的成功却难以找到。即使在动物研究中,尚不清楚是什么使干细胞衍生的外泌体发挥治疗作用。“这是我做的每一个演讲中提到的问题,”波士顿儿童医院团队研究员Gareth Willis说。他说“将外泌体视为管弦乐队而不是一种乐器。”蛋白质和RNA分子的组合可能比任何一种化合物都重要。
包括干细胞生物学家Raj Kishore在内的一些科学家希望阐明这一分子之谜。Kishore和他在天普大学的同事去年从国立卫生研究院获得了1160万美元的资助,用于研究心脏修复中干细胞衍生的外泌体。
“我们应该尝试更多地了解这种机制而不是急于治疗,”Kishore说。“我不希望看到这个领域像干细胞治疗领域一样死掉,因为不了解这些机制是如何运作的。”
即使学术实验室和生物技术公司开始使用外泌体来递送治疗剂或将囊泡用作治疗剂本身,它们也面临着一系列技术问题。马萨诸塞州综合医院的研究员Xandra O. Breakefield说:“制造足够量的囊泡是最大的挑战之一。” 现在,科学家们收集了从实验室培养的细胞中吐出的外泌体。“然后,当你得到你的囊泡,就如何分离它们存在很多不同意见。”
另一个问题是细胞外囊泡多样性。虽然研究人员曾经认识到两个主要类别,即外泌体和微泡,“现在我们意识到还有许多其他类型的囊泡,我们不知道如何分离它们,”Breakefield说。
约翰霍普金斯大学的Gould补充说:“这使很多人的实验变得复杂,”他也是Tavec制药公司的科学顾问,这是一家开发抗癌外泌体的初创公司。如果所有外泌体的大小不同并因此装载不同量的药物,则基于外泌体疗法的实验中的一致性和可重复性可能受到损害。
由于一些科学家正在研究从单一细胞系产生的多种外泌体,其他人正在寻求多样性。一家初创公司正在寻找来自细菌、真菌、植物和动物的新型外泌体。还有一组正在开发水果衍生的外泌体疗法来提供抗癌药物。
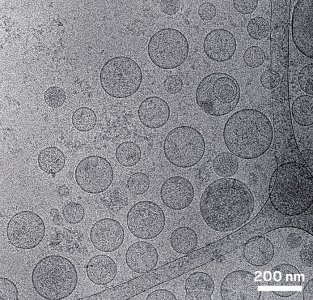
图片来源:Alain Brisson
如该电子显微照片所示,身体的大多数细胞释放各种尺寸大小的外泌体。
制药行业也开始关注。本月早些时候,罗氏同意向PureTech Health支付高达3600万美元的费用,用于获取从牛奶中提取的外泌体。“哺乳动物的乳汁中含有外泌体,”PureTech首席科学官Joseph Bolen说。
罗氏打算在外泌体中包装反义寡核苷酸用于口服递送。Bolen说,同样的方法可能适用于通常采用注射方法的其他核酸和生物疗法。“我们绝对相信这将得到广泛应用,”他说。
几乎所有从事外泌体治疗的人都在使用不同的外泌体来应对不同的疾病。他们正在快速地做到这一点。这可能有助于推动该领域向前发展,也有可能在出现问题时难以进行故障排除。Breakefield看到了外泌体基因治疗早期的阴影。
“对于这个领域来说,这是一个危险的时刻,”她说。“因为如果他们得到一些非常兴奋的结果,他们会非常自信地工作;而且事情一旦出了问题,它会让每个人都放弃。”
尽管如此,经历多年怀疑的科学家仍持乐观态度。“几乎没有人是刻意进入这个领域,” Gould说。相反,他认为向外泌体方法的转移是科学家追逐疾病的基本生物学、开发诊断或试图找到更好的药物输送方式的结果。
“这说明它们在生物学和医学的几乎每个方面都很重要,” Gould说。“这里潜力巨大。”
资料来源:美国化学学会(Ryan Cross)
外泌体资讯网 遇见外泌体,药物输送的后起之秀