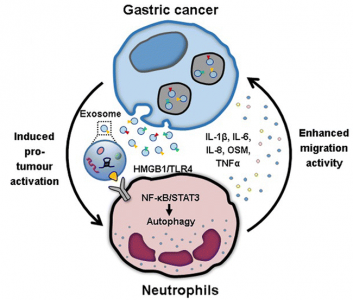
外泌体介导肿瘤与免疫细胞间的细胞通讯,中性粒细胞可被肿瘤细胞活化为促肿瘤表型,但肿瘤来源的外泌体在中性粒细胞调节中的功能仍不清楚。在这项发表于Molecular cancer杂志的研究中,来自江苏大学医学院的研究人员证明胃癌细胞通过外泌体诱导中性粒细胞的活化。胃癌细胞衍生的外泌体携带HMGB1蛋白,其与toll样受体4(TLR4)相互作用以激活NF-κB并诱导中性粒细胞中的自噬,进而促进胃癌细胞迁移。该研究结果表明外泌体是胃癌中性粒细胞活化的新调节因子。
中性粒细胞是肿瘤发展和进展的重要参与者。在各种肿瘤类型中,已显示中性粒细胞促进肿瘤发生、生长、转移、血管生成和免疫抑制。中性粒细胞产生遗传毒性物质,如活性氧(ROS),可破坏上皮细胞中DNA并引发癌变。中性粒细胞还可以产生多种因子,如中性粒细胞弹性蛋白酶(NE)和前列腺素E2(PGE2),促进肿瘤细胞增殖。此外,中性粒细胞可通过增强肿瘤细胞迁移和侵袭,降解细胞外基质,促进肿瘤细胞定植来促进肿瘤转移。同时,中性粒细胞损害免疫力以帮助肿瘤生长和转移。此外,中性粒细胞产生许多分子,如基质金属蛋白酶-9(MMP-9)和血管内皮生长因子(VEGF),以诱导血管生成。中性粒细胞浸润的增加和中性粒细胞/淋巴细胞比率升高(NLR)与肿瘤患者的疾病进展和预后不良有关。靶向中性粒细胞以抑制其促肿瘤功能已在小鼠模型中显示出治疗潜力。因此,更好地了解癌症中的中性粒细胞调节将为肿瘤诊断和治疗提供新的方法。
越来越多的研究表明,肿瘤会产生中性粒细胞相关的肿瘤微环境表型,从而有助于肿瘤进展。以往的研究表明,肿瘤细胞产生氧甾醇、CXCL5、透明质酸、粒细胞-巨噬细胞集落刺激因子(GM-CSF)、巨噬细胞移动抑制因子(MIF)等。这些因子诱导中性粒细胞的肿瘤前活化,导致肿瘤生长和转移增加。该研究团队此前已经报道来自肿瘤组织中的间充质干细胞的IL-6诱导中性粒细胞活化,导致血管生成和肿瘤转移增强。最近研究表明肿瘤浸润γδT细胞产生的IL-17可以募集、扩增和激活中性粒细胞,促进乳腺癌的肺转移。尽管如此,在肿瘤环境中调节中性粒细胞表型和功能的机制仍未完全被阐明。
外泌体是细胞来源的小脂质双层膜囊泡。外泌体作为细胞间通讯的新机制,可将生物活性分子从一个细胞穿梭到另一个细胞,从而形成遗传信息的交换和受体细胞的重编程。越来越多的证据表明肿瘤细胞释放过量的外泌体,促进肿瘤生长。此外,肿瘤来源的外泌体在肿瘤微环境中对免疫细胞发出信号,帮助肿瘤细胞逃避免疫监视并形成转移前微环境。最近表明,肿瘤细胞通过外泌体与间充质干细胞相互作用,促进肿瘤生长、转移和耐药。然而,肿瘤来源的外泌体在中性粒细胞活化中的功能尚未得到证明。
本研究中,研究人员探索了胃癌细胞衍生的外泌体(GC-Ex)对中性粒细胞的促肿瘤活化的影响,并阐明了潜在的机制。结果发现,GC-Ex延长中性粒细胞存活时间并诱导中性粒细胞中炎性因子的表达。GC-Ex激活的中性粒细胞促进胃癌细胞迁移。 GC-Ex转运HMGB1,通过与TLR4的相互作用激活NF-κB通路,导致中性粒细胞中的自噬反应增加。阻断HMGB1 / TLR4相互作用、NF-κB途径和自噬将会逆转GC-Ex诱导的中性粒细胞活化。沉默胃癌细胞中的HMGB1后,证实HMGB1是GC-Ex介导的中性粒细胞活化的关键因子。此外,HMGB1表达在胃癌组织中上调, HMGB1表达增加与胃癌患者预后不良有关。胃癌组织来源的外泌体在中性粒细胞活化方面与来自胃癌细胞系的外泌体作用基本一致。该研究证明胃癌细胞衍生的外泌体通过HMGB1 / TLR4 / NF-κB信号传导诱导中性粒细胞的自噬和促肿瘤活化,这提供了对肿瘤中性粒细胞调节机制的新见解,并阐明了外泌体在重塑肿瘤微环境中的多方面作用。
参考文献:Zhang X, Shi H, Yuan X, Jiang P, Qian H, Xu W. Tumor-derived exosomes induce N2 polarization of neutrophils to promote gastric cancer cell migration. Mol Cancer. 2018 Oct 6;17(1):146.