近日,中山大学孙逸仙纪念医院的宋尔卫、苏士成团队合作在Nature Cell Biology杂志在线发表了题为Extracellular Vesicle-packaged HIF-1α-stabilizing LncRNA from Tumour-associated Macrophages Regulates Aerobic Glycolysis of Breast Cancer Cells 的研究论文。该研究揭示巨噬细胞通过外泌体所包裹的lncRNA,调控肿瘤细胞的代谢重编程。
有氧糖酵解,也称为Warburg效应,葡萄糖主要加工成乳酸,是癌细胞中葡萄糖代谢的一般特征。虽然它在ATP生成中效率较低,但有氧糖酵解增加了生物合成,抑制细胞凋亡并产生信号代谢物,以在困难条件下增强癌细胞存活。有趣的是,已报道在各种恶性肿瘤中,包括非小细胞肺癌和乳腺癌,在实体瘤的不同区域中发现葡萄糖代谢的异质性。在肿瘤中心,缺氧使肿瘤细胞经历糖酵解,而有氧糖酵解也可在某些没有缺氧区域诱导。因此,可能存在不同的机制重新编程肿瘤的不同区域中的癌细胞的葡萄糖代谢。
众所周知,缺氧诱导因子-1(HIF-1)是氧传感转录因子,决定葡萄糖是通过氧化还是糖酵解消耗。在生理条件下,HIF-1α被脯氨酰羟化酶结构域2(PHD2)快速羟基化,并通过von Hippel-Lindau(VHL)结合经历泛素蛋白介导的蛋白酶体降解。然而,肿瘤微环境中的多种因素,如缺氧、活性氧、一氧化氮和某些代谢产物,可以调节PHD2的羟化酶活性,以防止HIF-1α降解,导致HIF-1α蛋白水平增加,并增强肿瘤细胞有氧糖酵解。
在癌症环境中,TAMs是最丰富的炎症细胞,并且与多种类型的癌症中的患者预后不良相关。 TAMs可以通过直接增强肿瘤细胞的恶性肿瘤来促进肿瘤进展,包括增殖、运动、侵袭性和化学抗性。然而,TAMs是否以及如何调节肿瘤细胞糖酵解,这对于它们在不良环境下的存活至关重要,目前尚不清楚。先前的研究已经表明,TAMs可以释放EVs,将microRNAs传递到邻近的肿瘤细胞中以调节它们的生物学功能。然而,关于在基质细胞和肿瘤细胞之间大于200个核苷酸的生物活性长链非编码RNA(lncRNA)的EVs传递的报道仍然缺乏。
来自中山大学孙逸仙纪念医院宋尔卫/苏士成团队合作的最新报道探究了TAMs是否参与调节大量浸润巨噬细胞的乳腺肿瘤区域的有氧糖酵解。此外,还研究了来自TAMs的EVs包装的lncRNAs在调节癌细胞的有氧糖酵解中的作用,并探索了潜在的机制。
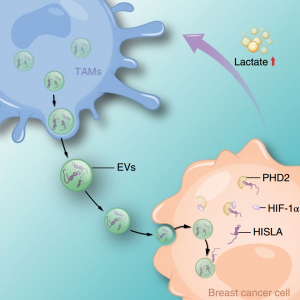
该研究证明肿瘤相关巨噬细胞(TAMs)通过包含lncRNA——HIF-1α稳定长非编码RNA(HISLA)——的细胞外囊泡(EVs)传递增强乳腺癌细胞的有氧糖酵解和细胞抗凋亡能力。机制上,HISLA阻断PHD2和HIF-1α的相互作用以抑制HIF-1α的羟基化和降解。相反,从糖酵解肿瘤细胞释放的乳酸上调巨噬细胞中的HISLA,构成TAMs和肿瘤细胞之间的前馈环。阻断EV传播的HISLA抑制体内乳腺癌的糖酵解和化学抗性。临床上,TAMs中的HISLA表达与糖酵解、化疗反应差和乳腺癌患者的生存期短有关。该研究强调了lncRNAs作为信号转导物的潜力,这些信号转导物通过EVs在免疫和肿瘤细胞之间传播,以促进癌症有氧糖酵解。
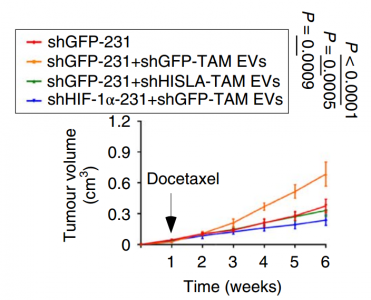
抑制巨噬细胞EVs中的lncRNA(HISLA)可显著减小肿瘤体积
改变肿瘤细胞代谢是改善癌症治疗的方案之一。该研究证明靶向TAMs特异性lncRNA抑制肿瘤细胞的糖酵解和细胞抗凋亡能力,突出了lncRNA在肿瘤治疗中成为有吸引力靶点的潜力。虽然有人已经提出抑制糖酵解酶的小分子抑制剂作为治疗方法,但仍然存在问题,因为它们不能区分由肿瘤和正常细胞表达的不同酶亚型。此外,抑制癌症特异性异构体可能诱导替代的其它亚型的过度表达,导致耐药性。研究已经表明RNA干扰介导的HISLA沉默可能提供更可行的方法来抑制肿瘤细胞的糖酵解。然而,siRNA递送的主要障碍是如何将小寡核苷酸靶向体内特定细胞类型。研究表明,适合细胞表面蛋白的核酸适体可用于将siRNA引入体内免疫细胞,包括巨噬细胞。因此,使用适体-siRNA嵌合体介导TAMs中特异性HISLA敲低用于癌症治疗的策略值得进一步研究。
参考文献:
Fei Chen, Jianing Chen, Linbin Yang, Jiang Liu, Xiaoqian Zhang, Yin Zhang, Qingqiang Tu, Dong Yin, Dechen Lin, Ping-Pui Wong, Di Huang, Yue Xing, Jinghua Zhao, Mengfeng Li, Qiang Liu, Fengxi Su, Shicheng Su & Erwei Song. Extracellular vesicle-packaged HIF-1α-stabilizing lncRNA from tumour-associated macrophages regulates aerobic glycolysis of breast cancer cells. Nature Cell Biology volume 21, pages498–510 (2019)