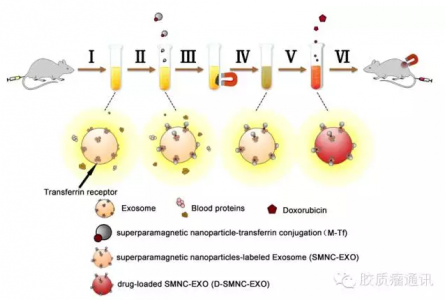
图1. 磁功能化外泌体的构建及其药物包载和投递的示意图
外泌体是一种由细胞分泌的天然纳米级(30-100nm)囊泡,由于其良好的生物相容性而被作为一种优异的药物和基因投递载体。然而,外泌体的临床应用受到现有外泌体的安全性低、分离纯化困难、靶向能力差等问题的制约。
如图1所示,该研究基于超顺磁性纳米粒子团簇的概念,利用转铁蛋白和转铁蛋白受体的特异性结合,将多个超顺磁性纳米粒子连接到同一个血液来源外泌体的表面。这种外泌体-超顺磁性纳米粒子的复合体(SMNC-EXOs)可以在外磁场的作用下迅速富集,又可在外磁场去除后很好的重分散;而且阿霉素后的SMNC-EXOs(D-SMNC-EXOs)进入动物体内后,可在外磁场的作用下实现对肿瘤部位的靶向,并释放阿霉素杀死肿瘤细胞。
图2. SMNC-EXOs的表征及其磁靶向能力的体外测定
透射电子显微镜及western blot结果证明SMNC-EXOs被成功制备(图2 A和B),而且SMNC-EXOs可在外加磁场的作用下迅速富集(图2C)。
图3. SMNC-EXOs的载药及体外细胞学评价
SMNC-EXOs可利用外泌体的磷脂双分子层包载疏水性药物阿霉素,而且偏酸性条件可加快D-SMNC-EXOs的阿霉素释放(图3 A和B)。D-SMNC-EXOs可被肿瘤细胞内吞,并释放阿霉素进入细胞核(图3C)。同时,D-SMNC-EXOs介导的阿霉素胞吞具有饱和性,当SMNC-EXOs的浓度达到一定量时,阿霉素的细胞吞噬效率不再变化,接近100%(图3D)。SMNC-EXOs并没有显著提高负载阿霉素的细胞毒性(图3E)。
图4. D-SMNC-EXOs的体内分布
D-SMNC-EXOs可在外加磁场的作用下,实现对肿瘤的靶向。这种靶向既包含SMNC-EXOs本身的被动靶向,又包含主动的磁靶向,从而有利于D-SMNC-EXOs逃避肝、脾、肾等器官的清除,实现阿霉素在肿瘤部位的富集(图4)。
图5. D-SMNC-EXOs的肿瘤治疗效果
D-SMNC-EXOs可提高阿霉素在肿瘤部位的富集,实现对小鼠肝癌H22皮下模型的有效抑制(图5)。
该研究利用超顺磁性纳米粒子团簇的概念,首次从血液中分离纯化得到外泌体并用于化疗药物的靶向投递。该方法得到的外泌体具有安全性高、分离纯化简单、靶向能力强等特点。此外,这种分离方式为外泌体在疾病诊断等方向提供了新的思路和方向。
参考文献:Hongzhao Qi, et al. Blood Exosomes Endowed with Magnetic and TargetingProperties for Cancer Therapy. ACS Nano 2016, accepted. DOI:10.1021/acsnano.5b06939
外泌体资讯网 磁功能化血液外泌体靶向肿瘤治疗的研究




