乳腺癌的早期诊断和精准治疗能够显著降低患者的死亡率。近年来,新型的液体活检标志物,如循环肿瘤细胞(CTCs),循环肿瘤DNA(ctDNAs)和肿瘤来源的细胞外囊泡(EVs),已经成为肿瘤研究的热点。其中,稳定富集大量不同的核糖核酸(RNA)的细胞外囊泡,可以反映其组织来源,可能适合作为液体活检标志物,用于肿瘤诊断和疗效预测。
2021年12月10日,来自复旦大学附属肿瘤医院吴炅教授、迟亚云副研究员和生物医学研究院黄胜林研究员的研究团队揭示了乳腺癌具有特征性的细胞外囊泡长链RNA谱(exLR profile),构建的诊断模型可用于早期乳腺癌的诊断。同时该团队发现细胞外囊泡特定内容物MSMO1 mRNA可用于乳腺癌新辅助疗效预测。相关内容以“Plasma extracellular vesicle longRNA profiles in the diagnosis and prediction of treatment response for breastcancer”为题发表在Nature旗下npj Breast Cancer杂志上 (2021, 7(1):154)。本文第一作者为复旦大学医学院博士研究生苏永辉和郭瑢、生物医学研究院博士研究生李玉琛。
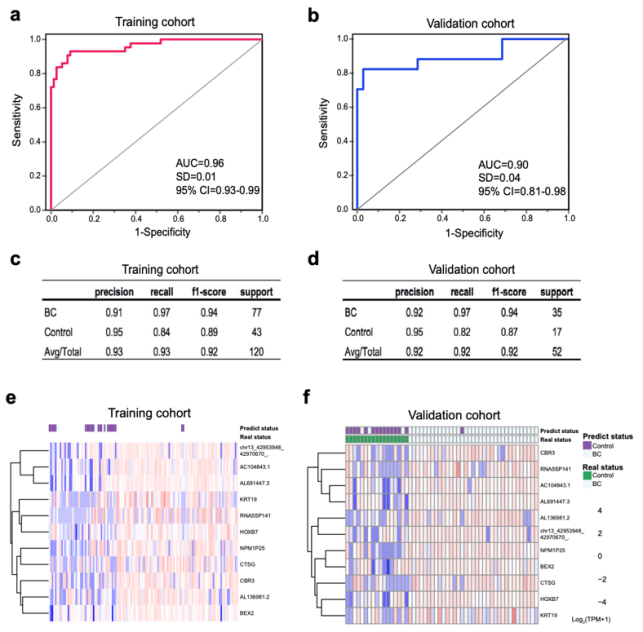
该研究首先对112例乳腺癌患者、19例良性乳腺病患者、41例健康对照者的血浆细胞外囊泡长链RNA进行测序,结果发现乳腺癌组与非癌症组相比,细胞外囊泡长链RNA的特征显著不同。通过Random Forest方法建立由11个长链RNA组成的乳腺癌诊断模型,具有较高准确性,训练队列、验证队列的真假阳性率曲线下面积分别达0.960、0.900 (图1),诊断早期(I或II期)乳腺癌的真假阳性率曲线下面积达0.940。而且,将该模型结合超声或钼靶等影像学检查,可以进一步提高乳腺癌诊断的准确性。
图1 细胞外囊泡长链RNAs用于乳腺癌的诊断
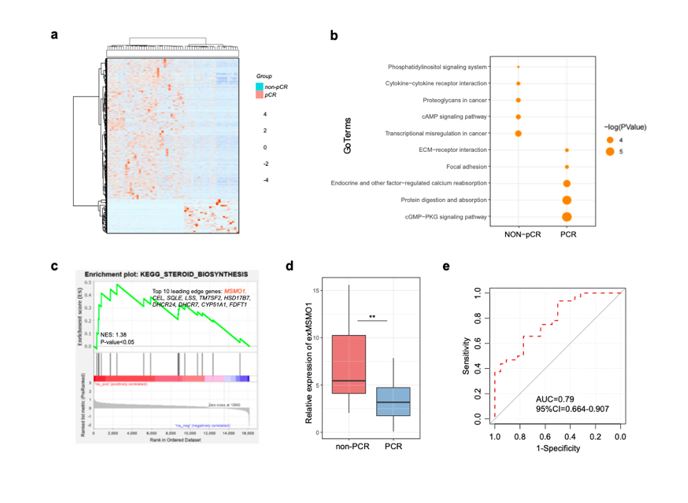
此外,该研究还入组了58例接受术前新辅助治疗的乳腺癌患者,发现治疗完全缓解组(pCR)和非完全缓解组(non-pCR)存在显著差异的exLRs靶点,并且类固醇生物合成通路(steroid biosynthesis pathway)在non-pCR组富集,该通路中的MSMO1 mRNA可以预测化疗后病理完全缓解与否,真假阳性率曲线下面积达0.790 (图2)。
图2 细胞外囊泡内MSMO1 mRNA用于乳腺癌新辅助疗效预测
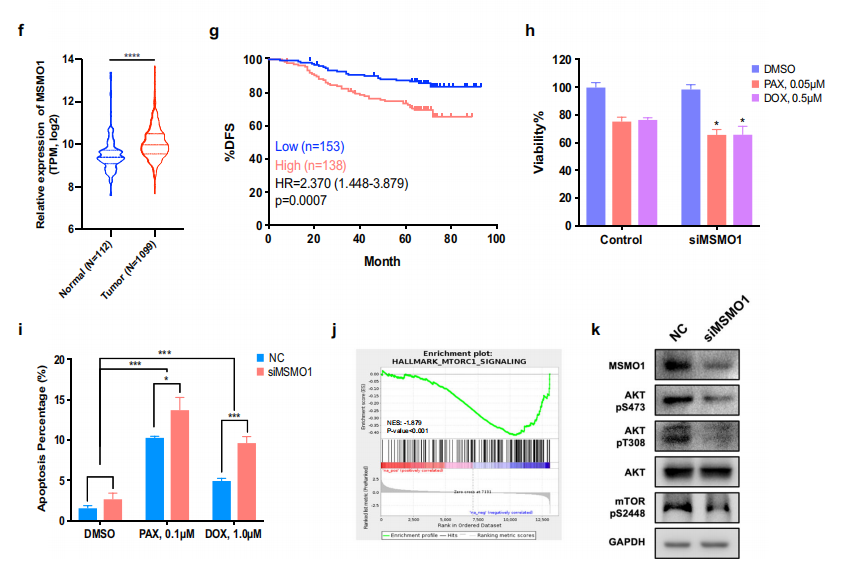
进一步研究发现MSMO1在乳腺癌组织中高表达,与病人预后相关,体外研究表明,抑制MSMO1表达,可以通过调节哺乳动物雷帕霉素靶蛋白复合物mTORC1信号传导通路,显著提高三阴性乳腺癌细胞MDA-MB-231对化疗药紫杉醇和多柔比星的敏感性(图3)。
图3 MSMO1在乳腺癌组织高表达,并与乳腺癌化疗敏感性相关
综上,该研究结果表明,细胞外囊泡长链RNA特征分析有望为乳腺癌早期诊断和疗效预测提供新的靶点。
参考文献:
Plasma extracellular vesicle long RNA profiles in thediagnosis and prediction of treatment response for breast cancer. npj Breast Cancer,2021, 10;7(1):154.